
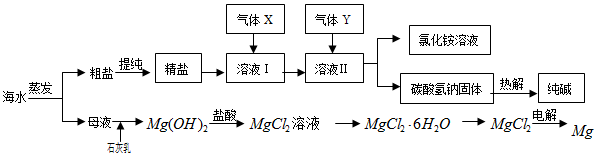
分析 将海水蒸发浓缩、冷却结晶得到粗盐和母液,向母液中加入Ca(OH)2,发生反应Mg2++2OH-=Mg(OH)2↓,过滤得到Mg(OH)2沉淀,将Mg(OH)2溶于稀盐酸中发生反应Mg(OH)2+2HCl=MgCl2+2H2O,将溶液蒸发浓缩、冷却结晶得到MgCl2.6H2O,将MgCl2.6H2O晶体在HCl氛围中加热得到固体
MgCl2,电解熔融氯化镁得到Mg,发生反应为MgCl2$\frac{\underline{\;通电\;}}{\;}$Mg+Cl2↑;
将粗盐提纯得到NaCl溶液,向溶液中通入氨气和二氧化碳,发生反应NaCl+NH3+CO2+H2O=NaHCO3+NH4Cl,碳酸氢钠溶解度小于NaCl而析出,所以得到溶液X为NH4Cl溶液,将NaHCO3加热发生反应2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O,最后得到碳酸钠固体,
(1)粗盐提纯是通过溶解把不溶物与食盐初步分离、过滤把不溶物彻底除去、蒸发把食盐从溶液中分离出来而得到食盐的过程;
(2)氨气溶解度大,二氧化碳溶解度小,先通入氨气会增大二氧化碳的吸收;
(3)根据碳酸钠的生产进行分析,向饱和食盐水中通入氨气再通入二氧化碳即可生成碳酸氢钠固体,碳酸氢钠受热分解即可得到碳酸钠;
(4)高温灼烧六水合氯化镁晶体(MgCl2•6H2O)所得固体是氧化镁,还有氯化氢和水蒸气,据此书写方程式.
解答 解:(1)将生成的硫酸钡、碳酸钡、碳酸钙、氢氧化镁沉淀从溶液中除去用过滤的方法;氯化钠和盐酸的混合溶液得到氯化钠晶体,可以用蒸发结晶的方法,除去溶液中的氯化氢和水,
故答案为:过滤;蒸发结晶;
(2)相同条件下,氨气的溶解度大于二氧化碳,为了提高二氧化碳的溶解度,先向饱和食盐水中通入氨气,故答案为:NH3;NH3的溶解度大,有利于提高产率;
(3)溶液Ⅱ中为氯化钠和氨水的混合液,为了提高二氧化碳的溶解度,加入二氧化碳后,NaCl、NH3、CO2等发生反应生成NaHCO3和NH4Cl,
故答案为:NaCl+NH3+CO2+H2O=NaHCO3↓+NH4Cl;
(4)从题意看出,高温灼烧六水合氯化镁晶体(MgCl2•6H2O)所得固体只有氧化镁,氯元素、氢元素和氧元素要成为氯化氢和水蒸气释放出去,该反应的化学方程式:MgCl2•6H2O$\frac{\underline{\;高温\;}}{\;}$MgO+2HCl↑+5H2O↑,
故答案为:MgCl2•6H2O$\frac{\underline{\;高温\;}}{\;}$MgO+2HCl↑+5H2O↑.
点评 本题以海水资源综合利用为载体考查了氧化还原反应、物质的分离和提纯、工艺流程等知识点,能从整体上把握工艺流程,知道物质间的反应、每一步的目的,题目难度中等.


科目:高中化学 来源: 题型:选择题
| 物质 | 选用试刘 | |
| A | NaBr溶液(NaI) | 溴水 |
| B | CuCl2溶液(FeCl3) | 铜粉 |
| C | 乙烷(乙烯) | 氢气 |
| D | 溴苯(苯) | 液溴 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 同质量的气体A与气体B,所含分子数目之比为a:b | |
| B. | 气体A与气体B的摩尔质量之比为a:b | |
| C. | 相同条件下,a g气体A与b g气体B体积之比为b:a | |
| D. | 相同条件下,气体A与气体B的密度之比为b:a |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 肼(N2H4)和氨是氮的两种常见化合物,在科学技术和生产中有广泛应用.回答下列问题:
肼(N2H4)和氨是氮的两种常见化合物,在科学技术和生产中有广泛应用.回答下列问题: .
.| T/℃ | 165 | 175 | 185 | 195 |
| K | 111.9 | 74.1 | 50.6 | 34.8 |
| n(N2) | n(H2) | n(NH3) | |
| 甲 | 1mol | 3mol | 0mol |
| 乙 | 0.5mol | 1.5mol | 1mol |
| 丙 | 0mol | 0mol | 4mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,44 g C3H8中含有的碳碳单键数为3NA | |
| B. | 标准状况下,22.4L 甲醇中含有的氧原子数为1NA | |
| C. | 1mol羟基中电子数为10NA | |
| D. | 在30 g甲醛和醋酸的混合物中,含有碳原子数为1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH3CH2CH3 | B. | CH3CH2CH2CH3 | C. | CH3COCH2CH3 | D. | 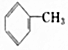 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
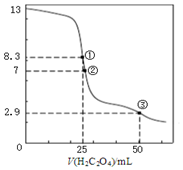 25℃时,用0.0500mol•L-1H2C2O4(二元弱酸)溶液滴定25.00mL0.1000mol•L-1NaOH溶液所得滴定曲线如图.下列说法不正确的是( )
25℃时,用0.0500mol•L-1H2C2O4(二元弱酸)溶液滴定25.00mL0.1000mol•L-1NaOH溶液所得滴定曲线如图.下列说法不正确的是( )| A. | 点①所示溶液中:c(H+)+2c(H2C2O4)+c(HC2O4-)=c(OH-) | |
| B. | 点②所示溶液中:c(HC2O4-)+2c(C2O42-)=0.0500mol•L-1 | |
| C. | 点③所示溶液中:c(Na+)>c(HC2O4-)>c(C2O42-)>c(H2C2O4) | |
| D. | 滴定过程中可能出现:c(Na+)>c(C2O42-)=c(HC2O4-)>c(H+)>c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com