
对某酸性溶液(可能含有Br-,SO ,H2SO3,NH
,H2SO3,NH )分别进行如下实验:
)分别进行如下实验:
①加热时放出的气体可以使品红溶液褪色;
②加碱调至碱性后,加热时放出的气体可以使润湿的红色石蕊试纸变蓝;
③加入氯水时,溶液略显黄色,再加入BaCl2溶液,产生的白色沉淀不溶于稀硝酸。
对于下列物质不能确认其在原溶液中是否存在的是( )
A.Br- B.SO C.H2SO3 D.NH
C.H2SO3 D.NH
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:

元素R、X、T、Z、Q在元素周期表中的相对位置如表所示,其中R单质在暗处与H2剧烈化合并发生爆炸。则下列判断正确的是( )
A.非金属性:Z<T<X
B.R与Q的电子数相差26
C.气态氢化物稳定性:R<T<Q
D.最高价氧化物的水化物的酸性:T>Q
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关系图中,A是一种正盐,B是气态氢化物,C是单质,F是强酸。当X无论是强酸还是强碱时都有如下转化关系(其他产物及反应所需条件均已略去),当X是强碱时,过量的B跟Cl2反应除生成C外,另一产物是盐酸盐。下列说法中不正确的是

A.B和Cl2反应是氧化还原反应
B.当X是强酸时,C在常温下是气态单质
C.当X是强酸时,A、B、C、D、E、F中均含同一种元素,F可能是H2SO4
D.当X是强碱时,A、B、C、D、E、F中均含同一种元素,F可能是HNO3
查看答案和解析>>
科目:高中化学 来源: 题型:
下列现象或事实不能用同一原理解释的是
A.浓硝酸和氯水用棕色试剂瓶保存
B.硫化钠和亚硫酸钠固体长期暴露在空气中变质
C.常温下铁和铂都不溶于浓硝酸
D.SO2和Na2SO3溶液都能使氯水褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
下列离子方程式正确的是( )
A.用食醋除去水壶内的水垢:CaCO3+2H+===Ca2++CO2↑+H2O
B.用惰性电极电解饱和氯化镁溶液:
2Cl-+2H2O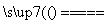 2OH-+H2↑+Cl2↑
2OH-+H2↑+Cl2↑
C.少量Cl2通入FeBr2溶液中:2Br-+Cl2===2Cl-+Br2
D.过量NaHSO4溶液加入到Ba(OH)2溶液中:
2H++SO +Ba2++2OH-===2H2O+BaSO4↓
+Ba2++2OH-===2H2O+BaSO4↓
查看答案和解析>>
科目:高中化学 来源: 题型:
写出下列反应的离子方程式:
(1)CO2气体溶于足量NaOH溶液。
(2)NaHCO3溶液与盐酸反应。
(3)少量NaOH溶液滴入Ca(HCO3)2溶液中。
(4)足量NaOH溶液滴入Ca(HCO3)2溶液中。
查看答案和解析>>
科目:高中化学 来源: 题型:
金属铜是人们最早使用的金属之一,下列关于铜电极的叙述不正确的是( )
A.铜锌原电池中铜是正极
B.用电解法精炼粗铜时粗铜做阳极
C.在镀件上镀铜时可用金属铜做阳极
D.电解水制H2、O2时铜做阳极
查看答案和解析>>
科目:高中化学 来源: 题型:
下图所示装置中,甲、乙、丙三个烧杯依次分别盛放100 g 5.00%的NaOH溶液、足量的CuSO4溶液和100 g 10.00%的K2SO4溶液,电极均为石墨电极。

(1)接通电源,经过一段时间后,测得丙中K2SO4质量分数为10.47%,乙中c电极质量增加。据此回答问题:
①电源的N端为________极;
②电极b上发生的电极反应为__________________________________________;
③电极b上生成的气体在标准状况下的体积为________L;
④电极c的质量变化是__________g;
⑤电解前后各溶液的pH是否发生变化:
甲溶液________________;乙溶液________________;
丙溶液________________;
(2)如果电解过程中铜全部析出,此时电解能否继续进行,为什么?
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com