
【题目】T℃时,A气体与B气体反应生成C气体。反应过程中A、B、C浓度变化如图(Ⅰ)所示,若保持其他条件不变,温度分别为T1 ℃和T2 ℃时,B的体积分数与时间的关系如图(Ⅱ)所示,则下列结论正确的是( )

A.该平衡体系的化学反应方程式为:A(g)+B(g)![]() C(g)
C(g)
B.(t1+10)min时,保持容器总压强不变,通入稀有气体,平衡向逆反应方向移动
C.T1<T2
D.其他条件不变,升高温度,正、逆反应速率均增大,且A的转化率增大
【答案】B
【解析】
A. 由图可知A、B为反应物,C为生成物,根据浓度的变化量之比等于化学计量数之比得到方程式;
B. (t1+10)min时,保持容器总压强不变,通入稀有气体,各物质的分压减小;
C. 根据先拐先平衡,数值大进行判断;
D.由II图可知,升高温度B的体积分数增大,即平衡逆向移动,正向为放热反应。
A. 由图可知A、B为反应物,C为生成物,A、B、C三种物质的浓度的变化量分别为:0.2mol/L、0.6mol/L、0.4mol/L,浓度的变化量之比等于化学计量数之比,因此可知方程式为:A(g)+3B(g)![]() 2C(g),A项错误;
2C(g),A项错误;
B. (t1+10)min时,保持容器总压强不变,通入稀有气体,各物质的分压减小,平衡向体积增大的方向移动,即平衡逆向移动,B项正确;
C. 先拐先平衡,数值越大,则有T1>T2,C项错误;
D. 由II图可知,升高温度B的体积分数增大,平衡逆向移动,则正向为放热反应,其他条件不变时,升高温度,正、逆反应速率均增大,但A的转化率减小,D项错误;
答案选B。


科目:高中化学 来源: 题型:
【题目】请解答下列与蛋白质有关的题目:
(1)鸡蛋腐烂时,常闻到有臭鸡蛋气味的气体,该气体中主要含有___________________(填化学式),说明蛋白质中含有___________________(填元素名称)元素。
(2)误食重金属盐会中毒,这是因为___________________。
(3)浓硝酸溅在皮肤上,使皮肤呈现___________________色,这是由于浓硝酸和蛋白质发生了___________________反应。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于离子方程式或离子共存的说法中正确的是![]()
A.向 ![]() 溶液中加入稀
溶液中加入稀 ![]() :
:![]()
B.![]() 溶液中加入足量
溶液中加入足量 ![]() 溶液:
溶液:![]()
C.某溶液中只存在以下 4种离子:![]() 、
、![]() 、
、![]() 、R离子
、R离子![]() 忽略微量的
忽略微量的 ![]() ,且浓度均为
,且浓度均为 ![]() ,则 R离子可能为
,则 R离子可能为 ![]()
D.![]() 的溶液中:
的溶液中:![]() 、
、![]() 、
、![]() 、
、![]() 能大量共存。
能大量共存。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁及其化合物在生活中有广泛应用。
(1)Fe2+基态的电子排布式为___。
(2)实验室用Fe3+检验苯酚。苯酚分子中碳原子的杂化方式为___。
(3)以Fe和BN为原料合成的铁氮化合物在光电子器材领域有广泛应用。
①以氨硼烷(NH3BH3)为原料可以获得BN。氨硼烷的结构式为___(配位键用“→”表示),氨硼烷易溶于水,其主要原因是___。
②以硼烷和氨气为原料可合成氨硼烷。NH3属于___分子(填“极性”或“非极性”)。
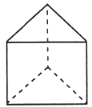
③如图为Fe与N所形成的一种化合物的基本结构单元,该化合物的化学式为___。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Co2O3常用于作氧化剂,在生产中有重要应用。
(1)一定条件下,0.996gCo2O3与15.00mL0.1mol·L-1的Na2S2O3溶液恰好完全反应,生成Co2+和一种含硫物质,该含硫物质中硫元素的化合价是___。
(2)Co2O3、PbO2、KMnO4均可与浓盐酸反应生成Cl2,同时分别生成Co2+、Pb2+和Mn2+。若生成等物质的量的Cl2,所需Co2O3、PbO2和KMnO4的物质的量之比为___。
(3)为测定某Co2O3样品中Co2O3的纯度(杂质不参与反应),现进行如下实验:
步骤1:称取样品2.000g于锥形瓶中,加入足量硫酸和50mL0.5000mol·L-1FeSO4溶液充分反应。
步骤2:向步骤1所得溶液中逐滴滴加0.0500mol·L-1KMnO4标准溶液至终点,消耗KMnO4标准溶液的体积为20.00mL。
已知步骤1、2中所涉及物质的转化分别为:Co3+![]() Co2+、MnO
Co2+、MnO![]()
![]() Mn2+
Mn2+
通过计算确定Co2O3样品中Co2O3的质量分数___(写出计算过程)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】人们对苯的认识有一个不断深化的过程。已知分子式为![]() 的甲、乙两种物质的结构简式如图所示。
的甲、乙两种物质的结构简式如图所示。

(1)甲、乙的化学性质的区别为甲能___________________(填字母,下同),而乙能___________________。
A.被酸性![]() 溶液氧化
溶液氧化
B.与溴水发生加成反应
C.与氢气发生加成反应
(2)![]() 甲和
甲和![]() 乙分别与
乙分别与![]() 发生完全加成反应,甲消耗___________
发生完全加成反应,甲消耗___________![]()
![]() ,而乙消耗__________
,而乙消耗__________![]()
![]()
(3)![]() 还可能有另一种结构丙(如图所示),其二氯代物有___________________种。
还可能有另一种结构丙(如图所示),其二氯代物有___________________种。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硒(Se)是第四周期ⅥA族元素,是人体内不可或缺的微量元素,其氢化物H2Se是制备新型光伏太阳能电池、半导体材料和金属硒化物的基础原料。
T℃时,向一恒容密闭容器中加入3molH2和lmolSe,发生反应H2(g)+Se(s)![]() H2Se(g)。
H2Se(g)。
①当反应达到平衡后,将平衡混合气体通入气体液化分离器使H2Se气体转化为液体H2Se,并将分离出的H2再次通入发生反应的密闭容器中继续与Se反应时,Se的转化率会提高。请用化学平衡理论解释___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式书写正确的是![]()
A.氯化钙溶液中通入![]() 气体:
气体:![]()
B.以石墨作电极电解氯化铝溶液:![]()
![]()
![]()
C.![]() 溶液中通入过量的
溶液中通入过量的![]() 气体:
气体:![]()
D.向明矾溶液中加入氢氧化钡溶液至沉淀的质量最大:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生活有密切联系,下列说法正确的是![]()
A.酸雨易导致土壤胶粒吸附![]() 使土壤酸化,影响铵态氮肥和钾肥的有效利用
使土壤酸化,影响铵态氮肥和钾肥的有效利用
B.汽车尾气污染物中含有氮的氧化物,是汽油不完全燃烧造成的
C.高纯度的单晶硅用于制造登月车的光电池和光导纤维
D.铝及其合金是电气、工业、家庭广泛使用的材料,通常用电解氯化铝的方法制取铝
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com