
【题目】下列实验方案中,能达到相应实验目的的是
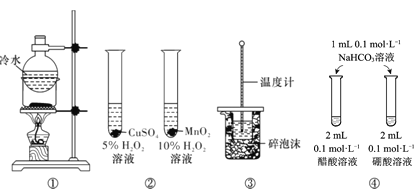
A.方案①用于分离I2和NH4Cl固体
B.方案用于比较CuSO4和MnO2的催化活性
C.方案③用于测定中和热
D.方案④用于比较醋酸和硼酸的酸性强弱
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】过滤在实验、生产、生活中有着广泛的应用。某研究性学习小组在实验室测定某含NaCl杂质的碳酸钠样品中Cl-的含量,其实验步骤如下:
①将100g样品溶于水得到溶液A。
②向A中加入稀HNO3酸化后,再加入沉淀剂B,使Cl-完全沉淀下来。
③进行如图所示操作,得到固体C,洗涤,干燥。

④称量得固体C的质量为2.87 g。
(1)沉淀剂B为________(填化学式)。
(2)向A中加入稀HNO3酸化的目的是_______________________。
(3)如何洗涤固体C: __________________。如果得到固体C后直接干燥、称量,会使样品中氯元素的质量分数________(填“偏大”“偏小”或“不变”)。
(4)该样品中氯元素的质量分数为________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醇与水蒸气重整可获得清洁能源,在催化剂作用下发生如下两步反应∶
反应①∶CH3OH(g)==CO(g)+2H2(g) △H1
反应②∶CO(g) + H2O(g)==CO2(g)+H2(g) △H2
根据能量变化示意图,下列说法不正确的是( )
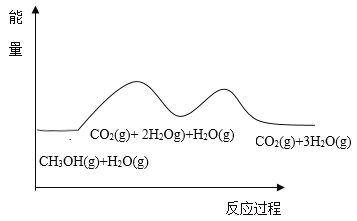
A.总反应的热化学方程式为∶ CH3OH(g)+H2O(g)=CO2(g)+3H2(g) ![]()
B.1mol CO(g)和1mol H2O(g)的总键能大于lmol CO2(g)和1mol H2(g)的总键能
C.甲醇与水蒸气催化重整的总反应速率取决于反应①
D.催化剂在反应中改变了活化能,加快了反应速率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应在常温下均为非自发反应,在高温下仍为非自发反应的是
A. Ag2O(s)===2Ag(s)+![]() O2(g)
O2(g)
B. Fe2O3(s)+![]() C(s)===2Fe(s)+
C(s)===2Fe(s)+![]() CO2(g)
CO2(g)
C. N2O4(g)===2NO2(g)
D. 6C(s)+6H2O(l)===C6H12O6(s)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)写出下列反应的离子方程式:
①硫酸和氢氧化钠溶液反应___;
②少量二氧化碳通入澄清石灰水___;
③碳酸钙和盐酸反应___;
④氯化钠和硝酸银反应___。
(2)写出符合下列离子反应的化学方程式:
①CO32-+Ba2+=BaCO3↓___;
②Cu2++Fe=Cu+Fe2+___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种3D打印机的柔性电池以碳纳米管作电极材料,以吸收ZnSO4溶液的有机高聚物为固态电解质,其电池总反应为:
![]() ,其电池结构如图1所示,图2是有机高聚物的结构片段。下列说法不正确的是
,其电池结构如图1所示,图2是有机高聚物的结构片段。下列说法不正确的是
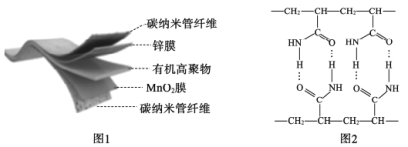
A.放电时,含有锌膜的碳纳米管纤维作电池负极
B.有机高聚物中含有的化学键有:极性键、非极性键和氢键
C.合成有机高聚物的单体是![]()
D.放电时,电极的正极反应为:MnO2+e-+H2O=MnOOH+OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知化学反应2C(s)+O2(g)![]() 2CO(g)、2CO(g)+O2(g)
2CO(g)、2CO(g)+O2(g)![]() 2CO2(g)都是放热反应。据此判断,下列说法不正确的是(其他条件相同)( )
2CO2(g)都是放热反应。据此判断,下列说法不正确的是(其他条件相同)( )
A.12g C所具有的能量一定高于28g CO所具有的能量
B.56 g CO和32 g O2所具有的总能量大于88 g CO2所具有的总能量
C.12 g C和32 g O2所具有的总能量大于44 g CO2所具有的总能量
D.将一定质量的C燃烧,生成CO2比生成CO时放出的热量多
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在装有MnO2的试管中加入H2O2可以快速制取O2,回答下列问题:
(1)H2O2中O的化合价是_____,写出H2O2中含有的化学键类型____(填字母序号)。
A.极性共价键 B.非极性共价键 C.离子键
(2)写出该反应的化学方程式 _______。
(3)MnO2的作用是______。
(4)下列措施可以加快该化学反应速率的是_______。
A.滴加FeCl3溶液 B.加热 C.降低压强 D.增大H2O2的浓度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃,在100mL0.1mol·L-1H2S溶液中,通入HCl气体或加入NaOH固体以调节溶液pH,溶液pH与c(S2-)关系如图(忽略溶液体积的变化和H2S的挥发)。下列说法正确的是( )
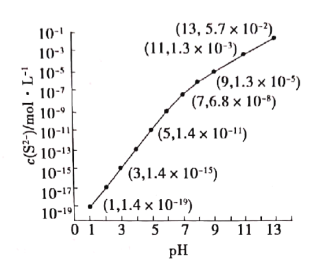
A.当c(H2S)+c(HS-)=0.043mol·L-1时,pH=13
B.pH=1时,c(H+)=c(Cl-)+c(HS-)+ c(S2-)+c(OH-)
C.向该溶液中加入NaOH固体至中性时c(Na+)>c(HS-)>c(S2-)>c(H+)=c(OH-)
D.已知:Ksp(MnS)=2.8×10-13,某溶液含amol·L-1Mn2+、0.10mol·L-1H2S,当溶液pH=5时,Mn2+开始沉淀,则a=0.2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com