
【题目】下列书写正确的是( )
A.在酸性碘化钾溶液中滴加双氧水:2I-+2H++H2O2===I2+2H2O
B.向NaHSO4溶液中滴加Ba(OH)2溶液至溶液呈中性:H++SO42-+Ba2++OH-===BaSO4↓+H2O
C.氢硫酸电离:H2S![]() 2H+ + S2-
2H+ + S2-
D.向稀HNO3中滴加Na2SO3溶液:SO32-+2H+===SO2↑+H2O
【答案】A
【解析】
A. 在酸性碘化钾溶液中滴加双氧水,双氧水具有强氧化性,与碘离子反应生成碘单质和水,离子方程式为2I-+2H++H2O2===I2+2H2O,符合题意,A正确;
B. 向NaHSO4溶液中滴加Ba(OH)2溶液至溶液呈中性:2H++SO42-+Ba2++2OH-===BaSO4↓+2H2O,与题意不符,B错误;
C. 氢硫酸为弱电解质,电离时部分电离,电离方程式为H2SH+ +HS-,与题意不符,C错误;
D. 向稀HNO3中滴加Na2SO3溶液,发生氧化还原反应,生成NO、硫酸根离子和水,离子方程式为3SO32-+2H++2NO3-== 3SO42-+2NO↑+H2O,与题意不符,D错误;
答案为A。


科目:高中化学 来源: 题型:
【题目】二氧化硅晶体是立体的网状结构,其结构如图所示。

下列关于二氧化硅晶体的说法不正确的是( )
A. 晶体中每个硅原子与4个氧原子相连
B. 晶体中硅、氧原子个数比为1∶2
C. 晶体中最小环上的原子数为8
D. 晶体中共用一个硅原子的最小的环的原子数目为12
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用CO和H2在催化剂的作用下合成甲醇,反应如下:CO(g)+2H2(g)=CH3OH(g)。在2L密闭容器中充入物质的量之比为1:2的CO和H2,在催化剂作用下充分反应.测得平衡混合物中CH3OH的体积分数在不同压强下随温度的变化如下图所示。下列说法正确的是

A.该反应的△H<O,且p1<p2<p3
B.在C点时,H2转化率为75%
C.反应速率:v逆(状态A)>v逆(状态B)
D.在恒温恒压条件下,向该密闭容器中再充入1molCH3OH,
达平衡时CH3OH的体积分数增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】《 Journal of Energy Chemistry》报导我国科学家设计CO2熔盐捕获与转化装置如图。下列有关说法正确的是

A. a为负极
B. 熔盐可用KOH溶液代替
C. d极电极反应式为CO32-+4e-===C+3O2-
D. 转移lmol电子可捕获CO211.2L(标况下)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数,下列说法正确的是( )
A.50mL 18.4mol/L浓硫酸与足量铜微热反应,生成SO2分子数目为0.46NA
B.2.3gNa与氧气完全反应,反应中转移的电子数介于0.1NA到0.2NA之间
C.用惰性电极电解饱和食盐水,若线路中通过NA 个电子,则阴极产生11.2L (标况)气体
D.已知N2(g)+3H2(g) ![]() 2NH3(g) ΔH=-92kJ·mol-1,现有0.1molN2与0.3molH2混合反应,可放热9.2kJ
2NH3(g) ΔH=-92kJ·mol-1,现有0.1molN2与0.3molH2混合反应,可放热9.2kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】盆烯是近年合成的一种有机物,它的分子结构可简化表示为![]() (其中C、H原子已略去),下列关于盆烯的说法中错误的是( )
(其中C、H原子已略去),下列关于盆烯的说法中错误的是( )
A. 盆烯是苯的一种同分异构体
B. 盆烯分子中所有的碳原子不可能在同一平面上
C. 盆烯是乙烯的一种同系物
D. 盆烯在一定条件下可以发生加成反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】次氯酸溶液是常用的消毒剂和漂白剂。某学习小组根据需要欲制备浓度不小于0.8mol/L的次氯酸溶液。
资料1:常温常压下,Cl2O为棕黄色气体,沸点为3.8℃,42 ℃以上会分解生成Cl2和O2,Cl2O易溶于水并与水立即反应生成 HClO。
资料2:将氯气和空气(不参与反应)按体积比1∶3混合通入潮湿的碳酸钠中发生反应2Cl2+2Na2CO3+H2O=Cl2O+2NaCl+2NaHCO3,用水吸收Cl2O(不含Cl2)制得次氯酸溶液。(装置及实验)用以下装置制备次氯酸溶液。

回答下列问题:
(1)各装置的连接顺序为_____→_____→_____→____→E。
(2)反应过程中,装置B需放在冷水中,其目的是_________________________。
(3)装置C的主要作用是______________________。
(4)若装置B中生成的Cl2O气体有20%滞留在E前各装置中,其余均溶于装置E的水中,装置E所得500mL次氯酸溶液浓度为0.8mol/L,则至少需要含水8%的碳酸钠的质量为_________g。
(5)已知次氯酸可被H2O2、FeCl2等物质还原成Cl-。测定E中次氯酸溶液的物质的量浓度的实验方案为:用________________准确量取20.00 mL次氯酸溶液,加入足量的________溶液,再加入足量的________溶液,过滤,洗涤,真空干燥,称量沉淀的质量。(可选用的试剂:H2O2溶液、FeCl2溶液、AgNO3溶液。)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸四氨合铜晶体([Cu(NH3)4]SO4·H2O)常用作杀虫剂、媒染剂。实验室拟用废旧印刷电路板(含有Cu、Fe、Al、Zn)制备该晶体,具体流程如下:

已知:硫酸四氨合铜易溶于水,不溶于乙醇、四氯化碳等有机溶剂;常温下,硫酸四氨合铜在空气中易与水和二氧化碳反应,受热时易失氨。
(1)某科研小组选取一定量的稀硝酸和稀硫酸的混合酸溶解废旧印刷电路板时,得出温度与铜的浸出率关系如图所示。步骤①中采用合适的加热方式是___;温度越高,铜的浸出率反而下降,原因可能是___。
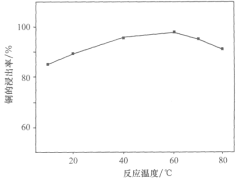
(2)步骤②、③需要的玻璃仪器有___;检验“水相Ⅱ”中是否含有Fe3+所需试剂为___。
(3)步骤④中氨水必须适当过量的原因是___。
(4)步骤⑥的具体操作为___。
(5)样品中NH3含量测定:实验装置如图所示,称取0.3400g样品放入圆底烧瓶中,加入80mL水溶解,再加入10%NaOH溶液10.00mL。在锥形瓶中,准确加入0.5000mol·L-lHC1标准溶液36.00mL,放入冰水浴中冷却。先大火后小火加热烧瓶,并保持微沸1h左右。取出插入HC1溶液中的导管,从冰水浴中取出锥形瓶,滴加2滴0.1%甲基红溶液,用0.5000mol·L-1NaOH标准溶液滴定剩余溶液,消耗NaOH标准溶液28.00mL。
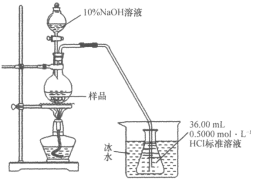
样品中NH3的质量分数为___(保留两位有效数字),实验检测结果比理论值偏小的原因可能是___(写一种可能原因)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D是中学化学常见的单质,甲、乙、丙为化合物,乙在常温常压下为无色无味的液体,元素A有可变化合价。它们之间存在如下图的所示的转化关系。由此推断:

(1)甲的化学式为_____________,丙的化学式为______________。
(2)写出甲和D反应的化学方程式___________________________________________。
(3)为检验化合物甲中元素的化合价,需要用到的药品有_________________________。
A.稀硫酸 B.盐酸 C.硫氰化钾溶液 D.高锰酸钾溶液
(4)为测定A和乙高温反应后所得固体中化合物甲的质量分数。取反应后所得固体并设计以下实验:

化合物甲的质量分数为________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com