
【题目】第ⅦA族元素具有相似的化学性质,其原因是它们的原子具有相同的
A. 电子层数 B. 核外电子数 C. 最外层电子数 D. 原子半径
科目:高中化学 来源: 题型:
【题目】下列能用勒夏特列原理解释的是( )
A. 高温及加入催化剂都能使合成氨的反应速率加快
B. 红棕色的NO2加压后颜色先变深后变浅
C. SO2催化氧化成SO3的反应,往往需要使用催化剂
D. H2、I2、HI平衡时的混合气体加压后颜色变深
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电解质溶液的电导率越大,导电能力越强。用0.1mol·L-1的NaOH溶液分别滴定体积均为10.00mL浓度均为0.1mol·L-1的盐酸和CH3COOH溶液,利用传感器测得滴定过程中溶液的电导率如图所示。
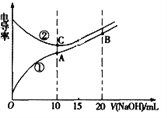
回答下列问题:
(1)曲线_______代表滴定CH3COOH溶液的曲线。
(2)在相同温度下,A、B、C三点溶液中水电离的c(H+)从大到小顺序为: ___________________。
(3)若室温下,当NaOH溶液滴定CH3COOH溶液恰好使溶液PH=7时, 消耗NaOH溶液为V L,则V取值应在 ___处,
A.0 – 5mL B.5 – 10mL C.10 –1 5mL D.15 – 20mL
CH3COOH溶液的电离平衡常数Ka用V表示为 Ka = _______(忽略混合时溶液体积的变化)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 苯和溴苯的混合物可用CCl4分离
B. 蛋白质和聚乙烯均属于天然有机髙分子化合物
C. 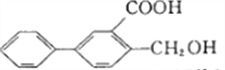 的苯环上的一氯代物有6种(不含立体异构)
的苯环上的一氯代物有6种(不含立体异构)
D. CH3CH2OH和 CH3CO18OH 发生酯化反应生成 CH3CO18OCH2CH3和H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由乙烷和乙醇蒸气组成的混和气体中,若碳元素的质量百分含量为60%,则氧元素的质量百分含量为
A. 15% B. 21% C. 25% D. 无法确定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】汽车尾气(主要成分为CO和NO)是形成雾霾的原因之一,对汽车尾气的处理也成为科学家研究的热点。
已知:I. N2(g)+O2(g) ![]() 2NO(g) ΔH= +180.7 IkJ mol-1;
2NO(g) ΔH= +180.7 IkJ mol-1;
Π . 2NO(g)+2CO(g) ![]() N2(g) + 2CO2(g) ΔH=-746.5 kj mol-1。
N2(g) + 2CO2(g) ΔH=-746.5 kj mol-1。
请回答下列问题:
(1)CO的燃烧热ΔH =____________。
(2)Ti℃时,向10 L容积不变的密闭容器中充人1 mol NO和1 mol CO,发生反应Π。5 min达到平衡时测得容器中CO2的物质的量为0.8 mol。则:
①05 min内,用N2表示的平均反应速率![]() (N2)=______________。 .
(N2)=______________。 .
②Ti℃时,该反应的平衡常数K=_______________。
③下列事实能说明该反应一定达到平衡状态的是______________(填选项字母)。
A.气体压强保持不变 B. ![]() 保持不变
保持不变
C.气体密度保持不变 D.速率之比:![]() =1
=1
④保持其他条件不变,平衡后再向该容器中充人1 mol NO、l molCO、0.5 mol N2、l molCO2,此时
![]() 正_______ (填“>”“<”或“ =”)
正_______ (填“>”“<”或“ =”) ![]() 逆
逆
(3)—定条件下,向密闭容器中充入一定量的N2、O2和CO,发生反应I和反应Ⅱ,容器中N2的平衡转化率(α)与溫度(T)和压强(p)的关系如图所示。则:

①α(N2)随温度升高而____________ (填“增大”或“减小”),理由为________________。
②M点和N点对应体系中,NO的体积分数:M______________ (填“>”“<”“ = ”)N。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用硝酸氧化淀粉水解的产物(C6H12O6)可以制备草酸,装置如下图所示(加热、搅拌和仪器固定装置均己略去)。
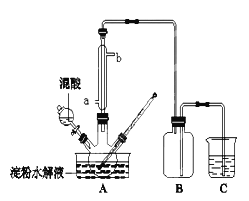
实验过程如下:
①将1∶1的淀粉水乳液与少许硫酸(98%)加入烧杯中,水浴加热至85℃~90℃,保持30 min,得到淀粉水解液,然后逐渐将温度降至60℃左右;
②将一定量的淀粉水解液加入三颈烧瓶中;
③控制反应液温度在55~60℃条件下,边搅拌边缓慢滴加一定量含有适量催化剂的混酸(65%HNO3与98%H2SO4的质量比为2:1.5)溶液;
④反应3h左右,冷却,减压过滤后得草酸晶体粗品,再重结晶得草酸晶体。
硝酸氧化淀粉水解液过程中可发生下列反应:
C6H12O6+12HNO3→3H2C2O4+9NO2↑+3NO↑+9H2O
C6H12O6+8HNO3→6CO2+8NO↑+10H2O
3H2C2O4+2HNO3→6CO2+2NO↑+4H2O
请回答下列问题:
(1)实验①加入少许98%硫酸的目的是:_____________________。
(2)冷凝水的进口是________(填a或b);实验中若混酸滴加过快,将导致草酸产量下降,其原因是______________________。
(3)装置B的作用是___________,为使尾气被充分吸收,C中的试剂是___________。
(4)重结晶时,将草酸晶体粗品经I加热溶解、Ⅱ趁热过滤、Ⅲ冷却结晶、Ⅳ过滤洗涤、Ⅴ干燥等实验步骤,得到较纯净的草酸晶体。该过程中可将粗品中溶解度较大的杂质在_________(填上述实验步骤序号)时除去;而粗品中溶解度较小的杂质最后留在_______(填“滤纸上”或“滤液中”)。
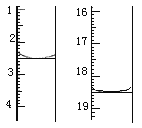
(5)将产品在恒温箱内约90℃以下烘干至恒重,得到二水合草酸。称取一定量该样品加适量水完全溶解,用KMnO4标准液滴定,反应的离子方程式为_________________。 滴定前后滴定管中的液面读数如图所示,则消耗KMnO4溶液的体积为_________。
(6)已知草酸是一种二元弱酸,草酸氢钠溶液(NaHC2O4)显酸性。常温下,向10 mL0.01 mol L -1IH2C2O4溶液中加入10mL0.01mol·L-1NaOH溶液时,溶液中各种离子的浓度由大到小的顺序为________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】若用AG表示溶液的酸度,其表达式为:AG=lg[![]() ]。室温下,实验室里用0.1 mol/L的盐酸溶液滴定10 mL 0.1 mol/L MOH溶液,滴定曲线如图所示:下列说法正确的是
]。室温下,实验室里用0.1 mol/L的盐酸溶液滴定10 mL 0.1 mol/L MOH溶液,滴定曲线如图所示:下列说法正确的是

A. 该滴定过程可选择酚酞作为指示剂
B. 若B点加入的盐酸溶液体积为5 mL,所得溶液中:c(M+) + 2c(H+) = c(MOH) + 2c(OH)
C. 滴定过程中从A点到D点溶液中水的电离程度:A<B<C<D
D. C点时加入盐酸溶液的体积等于10 mL
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com