
| A. | 该温度下,化学平衡常数K=0.1 | |
| B. | H2S的平衡转化率为20% | |
| C. | 增大CO浓度,平衡正向移动,可以提高CO的转化率 | |
| D. | 升高温度,H2S浓度增加,表明该反应正方向是吸热反应 |
分析 在1L恒容密闭容器中,加入10molCO、7molH2S,发生如下反应:CO(g)+H2S(g)?COS(g)+H2(g),达平衡时CO物质的量为8mol,说明反应转化了2molCO,则
CO(g)+H2S(g)?COS(g)+H2(g)
起始(mol) 10 7 0 0
转化(mol) 2 2 2 2
平衡(mol) 8 5 2 2
以此计算相关物理量并结合平衡移动的影响因素解答该题.
解答 解:在1L恒容密闭容器中,加入10molCO、7molH2S,发生如下反应:CO(g)+H2S(g)?COS(g)+H2(g),达平衡时CO物质的量为8mol,说明反应转化了2molCO,则
CO(g)+H2S(g)?COS(g)+H2(g)
起始(mol) 10 7 0 0
转化(mol) 2 2 2 2
平衡(mol) 8 5 2 2
A.因体积为1L,则浓度与物质的量数值相等,该温度下,化学平衡常数K=$\frac{2×2}{8×5}$=0.1,故A正确;
B.H2S的平衡转化率为$\frac{2}{7}$×100%=28.6%,故B错误;
C.增大CO浓度,平衡正向移动,但CO的转化率反而降低,故C错误;
D.升高温度,H2S浓度增加,说明平衡逆向移动,表明该反应逆方向是吸热反应,则正反应为放热反应,故D错误.
故选A.
点评 本题考查了化学平衡计算方法,为高频考点,侧重于学生的分析能力和计算能力的考查,注意把握该题计算的思路,把握外界条件下对平衡移动的影响,难度大.


 考前必练系列答案
考前必练系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 清晨的阳光穿过茂密的林木枝叶所产生的美丽景象(美丽的光线) | |
| B. | 尿毒症患者使用血液透析治疗 | |
| C. | 明矾净水 | |
| D. | 向FeCl3溶液中加入NaOH溶液,会出现红褐色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.08 | B. | 0.04 | C. | 0.032 | D. | 0.036 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 如图所示,图Ⅰ是恒压密闭容器,图Ⅱ是恒容密闭容器.当其它条件相同时,在Ⅰ、Ⅱ中都分别加入2molX和2molY,开始时容器的体积均为VL,发生如下反应并达到平衡状态:2X(?)+Y(?)?aZ(g).此时Ⅰ中X、Y、Z的物质的量之比为1:3:2.下列判断不正确的是( )
如图所示,图Ⅰ是恒压密闭容器,图Ⅱ是恒容密闭容器.当其它条件相同时,在Ⅰ、Ⅱ中都分别加入2molX和2molY,开始时容器的体积均为VL,发生如下反应并达到平衡状态:2X(?)+Y(?)?aZ(g).此时Ⅰ中X、Y、Z的物质的量之比为1:3:2.下列判断不正确的是( )| A. | 物质Z的化学计量数a=1 | |
| B. | 若X、Y均为气态,则在平衡时X的转化率:Ⅰ>Ⅱ | |
| C. | 若Ⅱ中气体的密度变化如图Ⅲ所示,则X、Y中只有一种为气态 | |
| D. | 若X为固态、Y为气态,则Ⅰ、Ⅱ中从开始到平衡所需的时间:Ⅰ>Ⅱ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
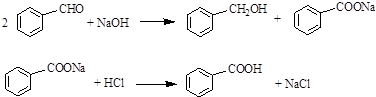
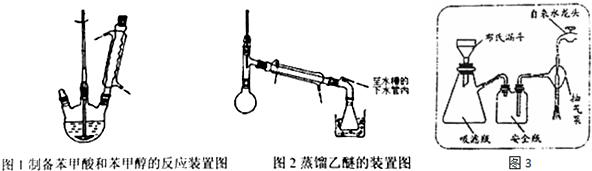
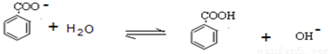 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| H2CO3 | H2SO3 | HNO2 | HClO |
| K1=4.4×10-7 K2=4.7×10-11 | K1=1.2×10-2 K2=6.6×10-8 | K=7.2×10-4 | K=2.9×10-8 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
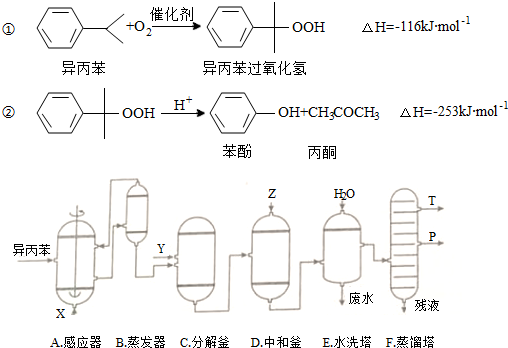
| 物质 | 相对分子质量 | 密度(g/cm-3) | 沸点/℃ |
| 异丙苯 | 120 | 0.8640 | 153 |
| 丙酮 | 58 | 0.7898 | 56.5 |
| 苯酚 | 94 | 1.0722 | 182 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将铁粉加入稀硫酸中:Fe+2H+═Fe2++H2↑ | |
| B. | NaHCO3溶液中加入HCl:CO32-+2H+═CO2↑+H2O | |
| C. | 用CH3COOH溶解CaCO3:CaCO3+2H+═Ca2++H2O+CO2↑ | |
| D. | MnO2与浓盐酸反应制Cl2:MnO2+4HCl═Mn2++2Cl-+Cl2↑+2H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com