
 铜及其化合物在工业、农业、科技和日常生活中有广泛应用.
铜及其化合物在工业、农业、科技和日常生活中有广泛应用.分析 (1)辉铜矿(主要成分是Cu2S)冶炼铜,和酸性高锰酸钾溶液反应生成铜离子,硫酸根离子,高锰酸根离子被还原为锰离子,结合原则守恒和电荷守恒配平书写;
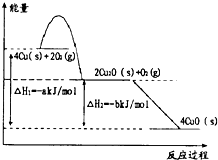
(2)①依据图象书写反应过程中的热化学方程式,结合个数定量计算所需热化学方程式;
②依据化学方程式灼烧后质量不变,反应的氧气和生成的二氧化碳和水的质量相同,结合金属生锈率=$\frac{已生锈的金属质量}{金属的总质量}$×100%,计算得到.
解答 解:(1)辉铜矿(主要成分是Cu2S)冶炼铜,和酸性高锰酸钾溶液反应生成铜离子,硫酸根离子,高锰酸根离子被还原为锰离子,铜元素化合价+1价变化为+2价,硫元素-2价变化为+6价,锰元素化合价+7价变化为+2价,依据电子守恒和原子守恒配平书写得到反应的离子方程式为:Cu2S+2MnO4-+8H+=2Cu2++SO42-+2Mn2++4H2O;
故答案为:1,2,8,2,1,2,4;
(2)①依据图象分析书写热化学方程式:①2Cu(s)+$\frac{1}{2}$O2(g)=2CuO(s)△H=-$\frac{a}{2}$KJ/mol,②2Cu2O(s)+O2(g)=4CuO(s)△H=-bKJ/mol;
依据盖斯定律计算(①×2-②)×$\frac{1}{2}$得到2Cu(s)+$\frac{1}{2}$O2(g)=Cu2O(s)△H=-($\frac{a-b}{2}$)kJ•mol-1;
故答案为:2Cu(s)+$\frac{1}{2}$O2(g)=Cu2O(s)△H=-($\frac{a-b}{2}$)kJ•mol-1;
②含有铜绿的铜片(假设不含其它杂质)在空气中灼烧至完全反应,经测定,反应前后固体的质量相同,说明反应的氧气质量和生成的二氧化碳、水蒸气的质量相同计算得到,设铜绿中铜物质的量为x,铜绿物质的量为y,
2Cu+O2$\frac{\underline{\;\;△\;\;}}{\;}$2CuO,
x 0.5x
Cu2(OH)2CO3$\frac{\underline{\;\;△\;\;}}{\;}$2CuO+CO2+H2O
y y y
0.5x×32=18y+44y
x:y=31:8
依据元素守恒计算,金属生锈率=$\frac{已生锈的金属质量}{金属的总质量}$×100%=$\frac{2y+64}{(2y+x)×64}$×100%=$\frac{2×\frac{8}{31}x×64}{(2×\frac{8}{31}x+x)×64}$×100%=34%;
故答案为:34%.
点评 本题考查了铜及其化合物性质分析判断,化学方程式计算应用,沉淀转化原理的应用,掌握基础是关键,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 100 g•mol-1 | B. | 108 g•mol-1 | C. | 55 g•mol-1 | D. | 96 g•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 混合溶液的pH值应等于7 | |
| B. | 如果酸是强酸,则pH一定小于7 | |
| C. | 如果碱是强碱,则pH一定不大于7 | |
| D. | 如果混合液的pH大于7,则碱一定为强碱 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| t/s | 0 | 2 | 4 | 6 | 8 |
| n(B)/mol | 0 | 0.30 | 0.39 | 0.40 | 0.40 |
| A. | 反应前2min的平均速率v(B)=0.15 mol/(L•min) | |
| B. | 保持其他条件不变,升高温度,平衡时c(B)=0.22 mol•L-1,则反应的△H<0 | |
| C. | 保持其他条件不变,起始向容器中充入2.0 mol A,反应达到平衡时C的体积分数减小 | |
| D. | 保持其他条件不变,增大该反应体系的压强,平衡左移,反应的平衡常数K减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 若温度不变,容器体积扩大一倍,此时A的浓度是原来的0.48倍,则a+b大于d | |
| B. | 若从正反应开始平衡时A、B的转化率相等,则A、B的物质的量之比为a:b | |
| C. | 若平衡体系中气体M mol,再充入bmolB,达到平衡气体量为(M+b)mol,则a+b=c+d | |
| D. | 若a+b=d,则当容器内温度上升时,平衡向左移动,容器中气体的压强不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 锌片逐渐溶解 | B. | 烧杯中溶液逐渐呈蓝色 | ||
| C. | 电子由铜片通过导线流向锌片 | D. | 电解质溶液的pH保持不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 研发易降解的生物农药 | |
| B. | 对燃煤进行脱硫处理 | |
| C. | 对塑料等垃圾进行深埋或倾倒入海处理 | |
| D. | 推广使用节能环保材料 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向豆浆中加入盐卤做豆腐 | |
| B. | 钢笔使用不同牌子的墨水堵塞 | |
| C. | 一束平行光线射入蛋白质溶液里,从侧面可以看到一束光亮的通路 | |
| D. | 向石灰水中通入二氧化碳气体产生白色浑浊 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 主要原料:碳酸钙 食用方法:每日一次,每次一片,嚼食. |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com