
| A.0. 4 mol·L-1 | B.0.6 mol·L-1 | C.0.9 mol·L-1 | D.1.2 mol·L-1 |
科目:高中化学 来源:不详 题型:单选题
 cC(g)+dD(g)ΔH同时符合下列两图中各曲线的规律的( )
cC(g)+dD(g)ΔH同时符合下列两图中各曲线的规律的( )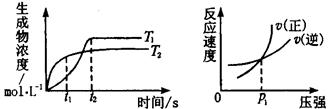
| A.a+b>c+d T1<T2 ΔH<0 |
| B.a+b>c+d T1<T2 ΔH>0 |
| C.a+b<c+d T1>T2 ΔH<0 |
| D.a+b>c+d T1>T2 ΔH>0 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| 时间(s) | 0 | 20 | 40 | 60 | 80 |
| n(NO2)/mol | 0.40 | n1 | 0.26 | n3 | n4 |
| n(N2O4)/mol | 0.00 | 0.05 | n2 | 0.08 | 0.08 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 CH3OH (g)+H2O(g) △H=-49.0 kJ/mol
CH3OH (g)+H2O(g) △H=-49.0 kJ/mol
| A.容器内各气体的体积比保持不变 | B.混合气体密度不变 |
| C.3v逆(CH3OH) =v正(H2) | D.H2转化率为75% |
 CO2(g) + 3H2(g)的平衡常数K= (计算结果保留2位小数)。
CO2(g) + 3H2(g)的平衡常数K= (计算结果保留2位小数)。查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 B(g)+C(g),在三种不同条件下进行,其中实验Ⅰ、Ⅱ都在800°C,实验Ⅲ在850°C,B、C的起始浓度都为0,反应物A的浓度(mol·L-1)随时间(min)的变化如图所示。
B(g)+C(g),在三种不同条件下进行,其中实验Ⅰ、Ⅱ都在800°C,实验Ⅲ在850°C,B、C的起始浓度都为0,反应物A的浓度(mol·L-1)随时间(min)的变化如图所示。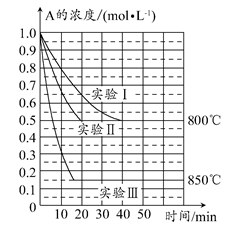
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 xC(g)+2D(g),经5 min后测得D的浓度为0.5 mol·L-1,c(A)∶c(B)=3∶5,用C的浓度变化表示的平均反应速率为0.1 mol·L-1·min-1。下列有关结论正确的是 ( )
xC(g)+2D(g),经5 min后测得D的浓度为0.5 mol·L-1,c(A)∶c(B)=3∶5,用C的浓度变化表示的平均反应速率为0.1 mol·L-1·min-1。下列有关结论正确的是 ( )查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 cC(g)△H="Q" kJ/mol,其化学平衡常数K和温度的关系如下表所示:
cC(g)△H="Q" kJ/mol,其化学平衡常数K和温度的关系如下表所示:
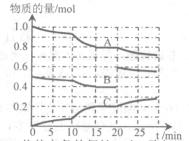
 (II)在恒定温度t℃,2L恒容密闭容器中发生反应aA(g)+bB(g) cC(g),容器中A、B、C物质的量变化如图所示,回答下列问题:
(II)在恒定温度t℃,2L恒容密闭容器中发生反应aA(g)+bB(g) cC(g),容器中A、B、C物质的量变化如图所示,回答下列问题:查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| 弱酸化学式 | CH3COOH | HCN | H2CO3 |
| 电离平衡常数(25℃) | 1.8×10-5 | 4.9×10-10 | K1=4.3×10-7 K2=5.6×10-11 |

 V3++VO2++H2O。则充电时阳极反应式为__________________________,用此电池电解1 L 1 mol·L-1的CuSO4溶液,当转移0.1 mol电子时,溶液的pH=________(不考虑溶液体积变化)。
V3++VO2++H2O。则充电时阳极反应式为__________________________,用此电池电解1 L 1 mol·L-1的CuSO4溶液,当转移0.1 mol电子时,溶液的pH=________(不考虑溶液体积变化)。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.0.2 mol·L-1·min-1 | B.0.1 mol·L-1·min-1 |
| C.0.04 mol·L-1·min-1 | D.0.08 mol·L-1·min-1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com