下列条件下,两瓶气体所含原子数一定相等的是( )
A.同体积、同密度的C2H4和C3H6
B.同质量的C2H4和CO
C.同温度、同体积的H2和N2
D.同压强、同体积的N2O和CO2
【答案】
分析:A、同体积、同密度的C
2H
4和C
3H
6,二者质量相等,二者最简式相同为CH
2;
B、C
2H
4和CO的摩尔质量相同为28g/mol,根据n=
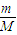
可知,二者质量相同,物质的量相同,但1个C
2H
4分子含有6个原子,1个CO分子含有2个原子;
C、同温度、同体积下,影响气体的物质的量的因素有压强,二者所处的压强不一定相同;
D、同压强、同体积下,影响气体的物质的量的因素有温度,二者所处的温度不一定相同.
解答:解:A、同体积、同密度的C
2H
4和C
3H
6,二者质量相等,二者最简式相同为CH
2,CH
2的物质的量相同,含有相同的原子数目,故A正确;
B、C
2H
4和CO的摩尔质量相同为28g/mol,根据n=

可知,二者质量相同,物质的量相同,但1个C
2H
4分子含有6个原子,1个CO分子含有2个原子,含有的原子数目之比为6:2=3:1,故B错误;
C、同温度、同体积下,影响气体的物质的量的因素有压强,二者所处的压强不一定相同,H
2和N
2都是双原子分子,若压强相同,含有的原子数目相同,若压强不同,含有原子数目不同,故C错误;
D、同压强、同体积下,影响气体的物质的量的因素有温度,二者所处的温度不一定相同,N
2O和CO
2都是三原子分子,若压强相同,含有的原子数目相同,若压强不同,含有原子数目不同,故D错误.
故选A.
点评:本题考查阿伏伽德罗定律及推论,难度中等,可以借助pV=nRT理解阿伏伽德罗定律及推论.

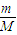 可知,二者质量相同,物质的量相同,但1个C2H4分子含有6个原子,1个CO分子含有2个原子;
可知,二者质量相同,物质的量相同,但1个C2H4分子含有6个原子,1个CO分子含有2个原子; 可知,二者质量相同,物质的量相同,但1个C2H4分子含有6个原子,1个CO分子含有2个原子,含有的原子数目之比为6:2=3:1,故B错误;
可知,二者质量相同,物质的量相同,但1个C2H4分子含有6个原子,1个CO分子含有2个原子,含有的原子数目之比为6:2=3:1,故B错误;
