
| A. |  含有两种溶质 | B. |  只含一种溶质 | ||
| C. | 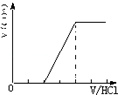 只含Na2CO3 | D. | 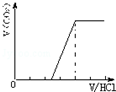 含有Na2CO3和 NaHCO3 |
分析 CO2与NaOH反应为①CO2+NaOH=NaHCO3,②CO2+2NaOH=Na2CO3+H20,
当$\frac{n(CO{\;}_{2})}{n(NaOH)}$≥1,反应按①进行,等于1时,CO2、NaOH恰好反应生成NaHCO3;大于1时,生成NaHCO3,CO2有剩余;
当$\frac{1}{2}$<$\frac{n(CO{\;}_{2})}{n(NaOH)}$<1,反应按①②进行,CO2、NaOH反应,无剩余,生成物为NaHCO3、Na2CO3;
当$\frac{n(CO{\;}_{2})}{n(NaOH)}$≤$\frac{1}{2}$,反应按②进行,等于$\frac{1}{2}$时,CO2、NaOH恰好反应生成Na2CO3;小于$\frac{1}{2}$时,生成Na2CO3,NaOH有剩余;
向M中逐滴加入盐酸,根据溶液M中溶质不同,再通过反应生成气体与消耗盐酸体积判断.
解答 解:CO2与NaOH反应为①CO2+NaOH=NaHCO3,②CO2+2NaOH=Na2CO3+H20,
当$\frac{n(CO{\;}_{2})}{n(NaOH)}$≥1,反应按①进行,等于1时,CO2、NaOH恰好反应生成NaHCO3;大于1时,生成NaHCO3,CO2有剩余;
当$\frac{1}{2}$<$\frac{n(CO{\;}_{2})}{n(NaOH)}$<1,反应按①②进行,CO2、NaOH反应,无剩余,生成物为NaHCO3、Na2CO3;
当$\frac{n(CO{\;}_{2})}{n(NaOH)}$≤$\frac{1}{2}$,反应按②进行,等于$\frac{1}{2}$时,CO2、NaOH恰好反应生成Na2CO3;小于$\frac{1}{2}$时,生成Na2CO3,NaOH有剩余;
A.由上述分析可知,当含有两种溶质,不论是Na2CO3、NaOH,还是NaHCO3、Na2CO3,滴加盐酸都不能立即产生气体,故A错误;
B.①当溶质为Na2CO3时,不能立即产生气体,滴加盐酸先与碳酸钠反应生成碳酸氢钠,碳酸氢钠再与盐酸发生反应生成二氧化碳,且与碳酸钠反应生成碳酸氢钠消耗盐酸体积等于与碳酸氢钠反应生成二氧化碳所消耗的盐酸体积,产生的气体体积V(CO2)与加入盐酸的体积V(HCl)的关系为 ;
;
②当溶质为NaHCO3时,滴加盐酸与碳酸氢钠反应生成二氧化碳,立即产生气体,产生的气体体积V(CO2)与加入盐酸的体积V(HCl)的关系为 ,故B错误;
,故B错误;
C.由B中分析可知,只含一种溶质,当溶质为Na2CO3时,产生的气体体积V(CO2)与加入盐酸的体积V(HCl)的关系为 ,故C正确;
,故C正确;
D.M含有含有Na2CO3和NaHCO3,与碳酸钠反应生成碳酸氢钠消耗盐酸体积小于与碳酸氢钠反应生成二氧化碳所消耗的盐酸体积,产生的气体体积V(CO2)与加入盐酸的体积V(HCl)的关系为 ,故D错误,
,故D错误,
故选C.
点评 本题考查混合物的有关计算,难度中等,关键判断溶液可能的溶质,分情况讨论,注意消耗盐酸的体积.


科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
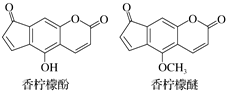 香柠檬油是从香柠檬树的果皮中提炼的橘子味的香油,33%的女用香水用到了这种原料.香柠檬油含微量的香柠檬酚和香柠檬醚,其结构如图.下列说法正确的是( )
香柠檬油是从香柠檬树的果皮中提炼的橘子味的香油,33%的女用香水用到了这种原料.香柠檬油含微量的香柠檬酚和香柠檬醚,其结构如图.下列说法正确的是( )| A. | 香柠檬醚的分子式为C13H6O4 | |
| B. | 香柠檬酚可与甲酸反应转化成香柠檬醚 | |
| C. | 1 mol香柠檬酚最多可与2 mol Br2发生反应 | |
| D. | 1 mol香柠檬酚最多可以与3 mol NaOH溶液反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C | B. | H2O | C. | H2 | D. | CO |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加入过量氨水,有白色沉淀生成,则原溶液中一定有Al3+ | |
| B. | 加入NaOH溶液然后加热,产生能使湿润的红色石蕊试纸变蓝的气体,则原溶液中一定有NH4+ | |
| C. | 加入用硝酸酸化的BaCl2溶液后有白色沉淀生成,则该无色溶液中一定含有Ag+ | |
| D. | 加入盐酸酸化的BaCl2溶液,有白色沉淀生成,则原溶液中一定有SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | v(NH3)=0.002mol/(L•s) | B. | v(O2)=0.01mol/(L•s) | ||
| C. | v(NO)=0.01mol/(L•s) | D. | v(H2O)=0.001mol/(L•s) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com