
分析 (1)①实验室用固体氯化铵和熟石灰粉末混合加热制取氨气,反应的化学方程式为:2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O;
②用浓氨水与NaOH固体或生石灰或碱石灰等混合可以迅速制备少量氨气;
③氨气极易溶于水,氯化铵对氨气的溶解性影响不大;
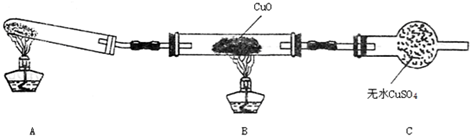
(2)①氯化铵和消石灰反应生成氨气和水,氨气和CuO反应前应先干燥,氨气有毒,需要完全吸收装置;
②由题意“CuO变为红色物质,无水CuSO4变蓝色,同时生成一种无污染的气体”可知生成物为铜、氮气和水,以此书写化学方程式;
(3)在酸性溶液中,Cu+能自身发生氧化还原反应生成Cu与Cu2+.
解答 解:(1)①实验室用氯化铵和消石灰反应生成氨气和氯化钙、水,反应的化学方程式为:2NH4Cl+Ca(OH)2 $\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O,
故答案为:2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O;
②用浓氨水与NaOH固体或生石灰或碱石灰等混合可以迅速制备少量氨气,
故答案为:NaOH固体(或生石灰或碱石灰等);
③氨气极易溶于水、氯化铵对氨气在水中的溶解影响不大,所以不能用用排饱和氯化铵溶液的方法收集氨气,
故答案为:否;
(2)①氯化铵和消石灰反应生成氨气和水,氨气和CuO反应前应先干燥,氨气有毒,会污染空气,多余的氨气不能直接排放,需要在C装置后需要连接尾气吸收装置,
故答案为:在装置A与B之间增加装有碱石灰的干燥管;C装置之后增加尾气吸收装置;
②CuO变为红色物质,该红色物质为Cu,无水CuSO4变蓝色,说明反应生成水,同时生成一种无污染的气体,根据质量守恒及化合价变化可知该气体为氮气,即:氧化铜与氨气反应生成铜、氮气和水,反应的化学方程式为:3CuO+2NH3$\frac{\underline{\;\;△\;\;}}{\;}$3Cu+N2+3H2O,
故答案为:3CuO+2NH3$\frac{\underline{\;\;△\;\;}}{\;}$3Cu+N2+3H2O;
(3)在酸性溶液中,Cu+能自身发生氧化还原反应生成Cu与Cu2+,检验该红色物质中是否含有Cu2O的实验方案为:取少量样品,加入稀H2SO4,若溶液出现蓝色,说明红色物质中含有Cu2O,反之,则没有,
故答案为:取少量样品,加入稀H2SO4,若溶液出现蓝色,说明红色物质中含有Cu2O,反之,则没有.
点评 本题考查氨气的制备方法及化学性质,题目难度中等,明确氨气的性质及实验基本操作方法是解题关键,试题侧重考查学生的分析、理解能力及化学实验能力.


科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C12H20O6 | B. | C15H26O6 | C. | C18H32O6 | D. | C21H38O6 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 常温下,将Cl2缓慢通入水中至饱和,然后向其中滴加0.1mol/LNaOH溶液.整个实验过程中溶液的pH变化曲线如图所示,不考虑次氯酸分解,下列叙述正确的是( )
常温下,将Cl2缓慢通入水中至饱和,然后向其中滴加0.1mol/LNaOH溶液.整个实验过程中溶液的pH变化曲线如图所示,不考虑次氯酸分解,下列叙述正确的是( )| A. | 实验过程中用pH试纸测定溶液的pH | |
| B. | a~b段,溶液中 $\frac{c({H}^{+})}{c(O{H}^{-})}$ 减小 | |
| C. | b点对应溶液中:c(Cl-)>c(H+)>c(HClO)>c(ClO-)>c(OH-) | |
| D. | c点对应溶液中:c(Na+)=c(Cl-)+c(ClO-) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 除去N2中的少量O2:通过灼热的铜网,收集气体 | |
| B. | 除 CO2中的少量HCl:通入饱和Na2CO3溶液,收集气体 | |
| C. | 除去FeCl3溶液中的少量FeCl2:加入足量铁屑,充分反应后过滤 | |
| D. | 除去NaCl溶液中的少量AlCl3:加入适量氨水,过滤 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 ②Na2O2
②Na2O2 ③N2
③N2 ④H2O
④H2O .
.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com