
������16�֣������ƾ���(Na2MoO4��2H2O)����������ȴˮϵͳ�Ľ�����ʴ�������⾫����Ҫ�ɷ���MoS2��������PbS�ȣ��Ʊ������ƾ���IJ����������£�
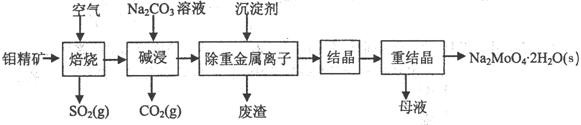 ��1�����յĹ����в��õ��ǡ��������ա��Ĵ�ʩ����ô�ʩ���ŵ��ǣ���_______________
��1�����յĹ����в��õ��ǡ��������ա��Ĵ�ʩ����ô�ʩ���ŵ��ǣ���_______________
��____________________________
��2��д������ʱ����MoO3�Ļ�ѧ����ʽΪ��______________________________________
��3��д�����������Ӧ�����ӷ���ʽ���� ��������������������
��4���ؽᾧ�õ���ĸҺ�������´��ؽᾧʱ�ظ�ʹ�ã����ﵽһ����������뾻��������ԭ���ǡ� ����������������������
��5����ͼ��̼����3�ֲ�ͬ�����еĸ�ʴ����ʵ������

��̼��������������и�ʴ���������Ũ�ȱ仯�����Բ��죬��ԭ������ǡ� ����________________��
�ڿ����������ζ�̼�ֵĻ�ʴԭ�����ڸ��������γ�FeMoO4��Fe2O3����Ĥ��
�ܱ�ʽѭ����ȴˮϵͳ�е�̼�ֹܵ���ʴ���������������������NaNO2����NaNO2�������ǡ�����_________________________________________��
�������ͼ������ơ��¹��ἡ������Ũ��Ϊ300mg��L��1����ʴЧ�����ʱ�����Ƶ����ʵ���Ũ��Ϊ������ ����
��6��﮺Ͷ������γɵĶ��ε�ص��ܷ�ӦΪ��xLi + nMoS2  Lix(MoS2)n�����طŵ�ʱ��������Ӧʽ�ǣ�___________________________________��
Lix(MoS2)n�����طŵ�ʱ��������Ӧʽ�ǣ�___________________________________��
��1���������⾫��������Ӵ���ʱ�䣬ʹ���ַ�Ӧ�����ԭ�ϵ������� ��1�֣�
��ʵ��������������Լ��Դ ��1�֣�
��2��2MoS2 + 7O2 = 2MoO3 +4 SO2 �����£���2�֣�
��3��MoO3��CO32��= MoO42����CO2�� ��2�֣�
��4�����ʹ�ú�ĸҺ�����ʵ�Ũ�������ٴ��ؽᾧʱ����������Ӱ���Ʒ���ȣ�2�֣�
��5����Cl��������̼�ֵĸ�ʴ��SO42��������̼�ֵĸ�ʴ��ʹ�ø����������еĸ�ʴ�������Կ��������1�֣�
������Һ����Ũ�ȵ�������������ǿ����ʹ�����ۻ�����ʴ���ʼ��� ��1�֣�
��������������������������� ��2�֣�
��7.28��l0��4mol��L��1 ��2�֣�
��6��nMoS2 + xLi+ + xe- = Lix(MoS2)n (2��)
��������
���������ҪŪ��ԭ�ϼ��Ʊ��IJ�Ʒ�����̵ĵ�һ�������ܿ�����
��1�����⡰�������ա��ڿα��ҵ����Ƶ�����������ˮ���������ķ�������ԣ�Ϊ������ȴЧ�����ã��ɴ˿�֪�����������ա���ȻҲΪ�����ӽӴ�ʱ�䣬���ԭ�����ʣ��Ӵ�ʱ�䳤����������Ҳ����֣��ܽ�Լ��Դ��
��2����д��MoS2 + O2 = MoO3 + ��һ���֣����ƶϳ���һ����Ϊ������������������ԭ��Ӧ��ʧ�����غ��ԭ���غ���ƽ��
��3�������ҵ��������������ͼ�е�λ�ã�ע�⣬��ͷָ����Ǽ�����Լ�����ָ�����Dz��������Na2CO3��������CO2������MoO42��Ӧ���������л�ȡ��Ϣ����MoO3��CO32��= MoO42����CO2��
��4���ؽᾧ��Ŀ�����ᴿ��Ʒ��ĸҺ��Ȼ����һ�����IJ�Ʒ��Ҳ����һ���������ʣ����Ե�һ���̶�ʱ��Ҫ���о�������Ϊ��������ʺ������ˡ�
��5���ٴ���һ��Ҫ����ͼ�к�����������������ʾ����ʲô������ͼ�п�֪����ͬ������£���ʴ���ʲ�һ������֪����ΪCl����SO42���IJ�ͬ���µģ�������Fe��Ũ�����Ũ�����л�ۻ������ԣ����������ʱ��Fe���淢���ۻ�Ҳ��ʹ��ʴ�����½���
���������Ƶ����ã�Ӧ��������ȥ�룬һ�������ԣ�����ǿ�������Σ�����������ĿӦ�õ��������ԡ�
��������ͼ�пɶ����������ơ��¹��ἡ����Ũ��Ϊ150 mg/L��150mg/Lʱ����ʴ��������͵ģ������Ƶ�Ũ��������Ũ�Ȼ�������ʵ���Ũ�ȼ��ɣ�(150��10-3g��206g/mol)��1L=7.28��l0��4mol��L��1
��6���ŵ�ʱ������Ӧ�Ƿ�����ԭ��Ӧ�ģ����ܷ�Ӧʽ���ҵ�������ԭ��Ӧ������ΪMoS2��������ԭ�IJ���ΪLix(MoS2)n����nMoS2+ e- + =Lix(MoS2)n,��������ȷ����������Li+�ĸ��������ݵ���غ㣬��������Li+�ĸ�������ȵģ��缫��ӦʽҲ������ˡ�
���㣺������ԭ��Ӧ�����ӷ�Ӧ����ʽ��д���缫��Ӧʽ����д�����ʵ���Ũ�ȵĻ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2013-2014�㶫ʡտ���и����꼶�ڶ���ģ�����ۻ�ѧ�Ծ��������棩 ���ͣ�ʵ����
��16�֣�ͭ��Ũ���ᷴӦ��ʵ��װ����ͼ��ʾ��
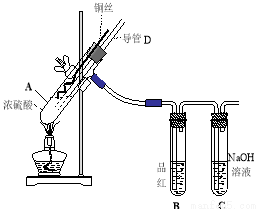
��1�� װ��A�з�����Ӧ�Ļ�ѧ����ʽΪ�� ����Ӧ�������Թ�B�е������� ���Թ�C�������� ��
��2�� ����D���¶�(���߶�)Ӧλ�� ��Һ���ϡ�Һ���£�������D�������У���ʵ��������ų�װ���е�SO2���� ��
ʵ���з����Թ��ڳ��˲�����ɫ�����⣬��ͭ˿���滹�к�ɫ��������ɣ����п��ܺ���CuO��Cu2O��CuS��Cu2S��Ϊ̽���ijɷ֣����������µ�ʵ�顣
�������Ͽ�֪��Cu2O + 2HCl =CuCl2 + Cu + H2O�� 2Cu2O + O2���� 4CuO��2CuS+3O2����2CuO+2SO2 ��Cu2S+2O2����2CuO+SO2 ��CuS�� Cu2S��ϡHCl����Ӧ��
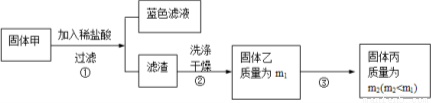
��3�� �������ڿ���������ʱ��ʹ�õ�ʵ���������˲����������żܡ��ƾ����⣬�������У� ��
��4�� ���չ����У���������Ӧ�⣬�����ܷ�����Ӧ�ķ���ʽΪ ��
��5�����ۣ�������CuO�����϶����е������� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014�㶫ʡ��һѧ�����տ��Ը�һ����ѧ���Ծ��ң������棩 ���ͣ�ѡ����
a��CO��O2�Ļ�����壬��ȼ��õ�b�����壨ǰ��������ͬ��������������CO�������������������е� �� ��
��b ��2a/3 ��a��b ��a��b ��2(a��b)
A���٢ڢ� B���ڢܢ� C���٢ڢ� D���٢ڢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014�㶫ʡ�����и߿�Ԥ�����ۻ�ѧ�Ծ��������棩 ���ͣ������
������16�֣���ˮAlCl3�������л��ϳɵĴ�����ʳƷ���ɼ��ȡ���ҵ�Ʊ���ˮAlCl3���������£�

��1���Ȼ�¯��ͨ��O2��Ŀ���� _________��
��2���Ȼ�¯��Al2O3��C12��C��Ӧ�Ļ�ѧ����ʽ��____________________________��
��3���Ȼ�¯�е��������壬ͨ��������������Һ�����գ���д����Na2SO3��Һ����β��ʱ������Ӧ�����ӷ���ʽ___________________________________________________��
��4�����������м������۵�Ŀ����_________________________________________��
��5�����Ȼ������壨AlCl3��6H2O����HCl���м���Ҳ�ܽ�����ˮ�Ȼ������Ʊ�������ʵ���������Ʋ��������յõ��������Ǽ�ʽ�Ȼ���[��ѧʽΪAl2(OH)nCl(6-n)]����������ԭ�Ȼ������壨AlCl3��6H2O����40%���������n��ֵΪ ��
��6�����������У�������Ϊ�����������ε��Һ����Ԫ����Ҫ��AlCl4����ʽ���ڣ��������ĵ缫��ӦʽΪ___________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014�㶫ʡ�����и߿�Ԥ�����ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
����ʵ����������߱仯����ȷ����
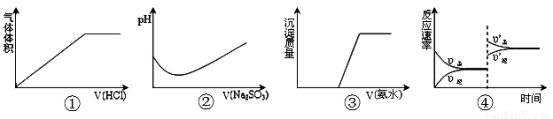
A���ٱ�ʾNa2CO3��Һ�е���ϡ����
B���ڱ�ʾ��ˮ�е���Na2SO3��Һ
C���۱�ʾHCl��MgCl2��Һ�е��백ˮ
D���ܱ�ʾһ�������·�Ӧ:2SO2+O2 2SO3 ��H< 0 ����ƽ�������ѹǿ
2SO3 ��H< 0 ����ƽ�������ѹǿ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014�㶫ʡ�߿�Ԥ�����ۻ�ѧ�Ծ����������棩 ���ͣ�ѡ����
��55��ʱ������˵����ȷ����
A����ˮ�м��������������ƹ��壬�ٽ���ˮ�ĵ��룬c(H+)����Kw����
B��pH=8��NaHCO3��Һ�У�c(OH-)=1��10-6mol/L
C��������ˮ�У�c(Cl2)=2c(ClO��)+2c(Cl��)+2c(HClO)
D��0.1mol/L��(NH4)2SO4��Һ�У�c(NH4+) > c(SO42-) > c(H+) > c(OH-)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014�㶫ʡ�����и߶����в������ۻ�ѧ�Ծ��������棩 ���ͣ������
��ҵ������ij�����ķ���(��Ҫ��CuO70%��MgFe2O420%������������FeO��NiO��������)��ȡ��ͭ���������졣������ͼ��ʾ��
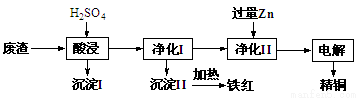
�ش��������⣺
��1�������������������
��һ���ǽ���Һ��������Fe2��������
�ڶ����ǿ�����ҺpH��ʹFe3��ת��ΪFe(OH)3������
��д��������������H2O2����Fe2����Ӧ�����ӷ���ʽ�� ��
��25 ��ʱ��pH=3����Һ�У�c(Fe3��)=___________mol��L��1����֪25 �棬Ksp[Fe( OH)3]=4.0��10��38����
�۾������еڶ�����ѡ��CuOʵ��ת�����û�ѧƽ���ƶ�ԭ��˵����ԭ��
��
��2���þ���II���õĽ���Ϊ�缫���е��þ�ͭ����д�������������ĵ缫��Ӧʽ��______________________________��
��3��Ϊȷ�ⶨ���Һ��Fe2�������ʵ���Ũ����ȷ��H2O2���������ⶨ�������£�
��ȡ��25.00mL���Һ�����Ƴ�250.0mL��Һ��
�ڵζ���ȷ��ȡ25.00mL������Һ����ƿ�У���0.2000mol/LKMnO4��Һװ��
�����������ƣ������еζ�����¼���ݣ��ظ��ζ�3�Σ�ƽ������KMnO4��ҺV mL��(��Ӧ���ӷ���ʽ��5Fe2++MnO +10H+=5Fe3++Mn2++5H2O)
+10H+=5Fe3++Mn2++5H2O)
�ۼ������Һ��Fe2+�����ʵ���Ũ��= mol/L ��ֻ�г���ʽ���������㣩��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014�㶫ʡ÷���и�һ��ѧ�����л�ѧ�Ծ��������棩 ���ͣ�ѡ����
������ʵһ�㲻�������жϽ�����ǿ�����ǣ� ��
A.��������ɫ���۷е�
B.����Ԫ�ص�����������Ӧ��ˮ����ļ���ǿ��
C.1mo���������ڷ�Ӧ��ʧȥ���ӵĶ���
D.����Ԫ�صĵ��ʺ�ˮ�����û����������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014�㶫ʡ�����и�һ��ѧ����ĩ���Ի�ѧ�������Ծ��������棩 ���ͣ�ѡ����
��֪��ӦA2��g��+2B2��g�� 2AB2��g����H ��0������˵����ȷ��
2AB2��g����H ��0������˵����ȷ��
A�������¶ȣ�����Ӧ�������ӣ�����Ӧ���ʼ�С
B�������¶������ڷ�Ӧ�������ӣ��Ӷ����̴ﵽƽ���ʱ��
C���ﵽƽ��������¶Ȼ�����ѹǿ�������ڸ÷�Ӧƽ�������ƶ�
D���ﵽƽ������¶Ȼ��Сѹǿ�������ڸ÷�Ӧƽ�������ƶ�
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com