
下图是一种航天器能量储存系统原理示意图。
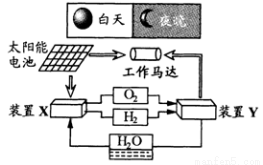
下列说法正确的是
A.该系统中只存在3种形式的能量转化
B.装置X能实现燃料电池的燃料和氧化剂再生
C.装置Y中负极的电极反应式为:O2 + 2H2O + 4e- = 4OH-
D.装置X、Y形成的子系统能实现物质的零排放,并能实现化学能与电能间的完全转化
科目:高中化学 来源:2015-2016学年湖南省益阳市高一下期末化学试卷(解析版) 题型:选择题
为提纯下列物质(括号内为杂质),所用的除杂试剂和分离方法都正确的是( )
序号 | 不纯物 | 除杂试剂 | 分离方法 |
A | CH4(C2H4) | 酸性KMnO4溶液 | 洗气 |
B | 苯(Br2) | NaOH溶液 | 过滤 |
C | C2H5OH(H2O) | 新制生石灰 | 蒸馏 |
D | 乙酸乙酯(乙酸) | 饱和Na2CO3溶液 | 蒸馏 |
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山东省济宁市高一下期末化学试卷(解析版) 题型:填空题
四种短周期元素A、B、C、D的性质或结构信息如下:
信息:①原子半径:A>B>C>D ②四种元素之间形成的某三种分子的比例模型及部分性质如下:
甲: 是地球上最常见的物质之一,是所有生命体生存的重要资源,约占人体体重的三分之二。
是地球上最常见的物质之一,是所有生命体生存的重要资源,约占人体体重的三分之二。
乙: 无色,无气味并且易燃。是常见的一种基础能源。
无色,无气味并且易燃。是常见的一种基础能源。
丙: 有强氧化性的弱酸,可以用于消毒杀菌。
有强氧化性的弱酸,可以用于消毒杀菌。
请根据上述信息回答下列问题。
(1)B元素在元素周期表中的位置为________________,请写出BC2分子的电子式:_______________。
(2)A所在周期中,E元素的单质还原性最强,F元素的某些盐类常用作净水剂。E单质与甲反应有化合物X生成。请写出以下两个反应的离子方程式:
①A元素的单质与物质甲发生反应:_____________________________________。
②F、C两种元素组成的化合物Y可作为高温结构陶瓷材料,X与Y两种化合物在溶液中发生反应:______________________________________________________。
(3)物质丁的元素组成和甲相同,丁分子具有18电子结构。向盛有一定浓度丁溶液的试管中,逐滴加入硫酸酸化的硫酸亚铁溶液。滴加过程中的现象为:
①试管中溶液变成深棕黄色,发生反应的离子方程式为 ;
②开始有少量气泡出现(经验证是氧气),片刻后反应变得剧烈,继续滴加溶液,静置一段时间,试管底部出现红褐色沉淀。请回答“片刻后反应变得剧烈”的原因是a b
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山东省济宁市高一下期末化学试卷(解析版) 题型:选择题
下列有关说法正确的是
A.蛋白质和油脂都属于高分子化合物,一定条件下都能水解
B.医疗上可用硫酸钡作x射线透视肠胃的内服药,是因为硫酸钡不溶于水
C.用过滤的方法从碘的四氯化碳溶液中获得碘
D.用浓硫酸配制一定物质的量浓度的稀硫酸时,浓硫酸溶于水后,应冷却至室温才能转移到容量瓶中
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山东省济宁市高二下期末化学试卷(解析版) 题型:填空题
煤燃烧排放的烟气中(主要含SO2、CO2)的SO2形成酸雨、污染大气,对烟气进行脱硫,回答下列问题:
(1)采用Ca(ClO)2烟气脱硫可得到较好的效果。已知下列反应:
①SO2(g)+2OH? (aq) =SO32? (aq)+H2O(l) ΔH1
②ClO? (aq)+SO32? (aq) =SO42? (aq)+Cl? (aq) ΔH2
③CaSO4(s) =Ca2+(aq)+SO42?(aq) ΔH3
则反应SO2(g)+ Ca2+(aq)+ ClO? (aq) +2OH? (aq) = CaSO4(s) +H2O(l) +Cl? (aq)的ΔH=_ 。
(2)采用氨水烟气脱硫,最终可得到氮肥。将相同物质的量的SO2与NH3溶于水所得溶液中c(H+)﹣c(OH-)= (填字母编号).
A.c(SO32-)﹣c(H2SO3)
B.c(SO32-)+c(NH3·H2O)﹣c(H2SO3)
C.c(HSO3-)+c(SO32-)﹣c(NH4+)
D.c(HSO3-)+2c(SO32-)﹣c(NH4+)
(3)烟气在较高温度经下图方法脱除SO2,并制得H2SO4。
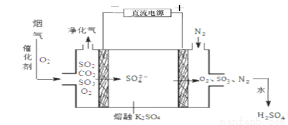
①在阴极放电的物质是 。
②在阳极生成SO3的电极反应式是 。
③已知室温下,Ksp(BaSO4)=1.1×10-10。将脱除SO2后制得的H2SO4配成pH=4 的H2SO4溶液,与pH=9的 Ba(OH)2 溶液混合,若所得混合溶液的 pH=7,则 Ba(OH)2 溶液与 H2SO4 溶液的体积比为 。欲使溶液中c(SO42-) =2.0×10-4mol·L-1,则应保持溶液中 c(Ba2+) = mol·L-1。
(4)一定条件下,用Fe2O3、NiO或Cr2O3作催化剂,利用如下反应回收燃煤烟气中的硫。反应为:2CO(g)+SO2(g) 2CO2(g)+S(l) ΔH= - 270KJ·mol-1其他条件相同、催化剂不同时,SO2的转化率随反应温度的变化如图1,不考虑催化剂的价格因素,选择_ 为该反应的催化剂较为合理(选填序号)。
2CO2(g)+S(l) ΔH= - 270KJ·mol-1其他条件相同、催化剂不同时,SO2的转化率随反应温度的变化如图1,不考虑催化剂的价格因素,选择_ 为该反应的催化剂较为合理(选填序号)。
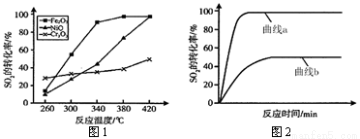
a. Cr2O3 b. NiO c. Fe2O3
选择该催化剂的理由是:_ 。
某科研小组用选择的催化剂,在380℃时,研究了n(CO) : n(SO2)分别为1:1、3:1时,SO2转化率的变化情况(图2)。则图2中表示n(CO) : n(SO2)=3:1的变化曲线为 。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山东省济宁市高二下期末化学试卷(解析版) 题型:选择题
下列热化学方程式及有关应用的叙述中,正确的是
A.甲烷的燃烧热为890.3kJ·mol-1,则甲烷燃烧的热化学方程式可表示为:
CH4(g)+2O2(g)=CO2(g)+2H2O(g) △H= -890.3kJ·mol-1
B.已知强酸与强碱在稀溶液里反应的中和热为57.3 kJ·mol-1, 则1/2 H2SO4(aq)+1/2 Ba(OH)2(aq)= 1/2BaSO4(s)+H2O(l) ΔH= -57.3 kJ·mol-1
C. 500℃、30MPa下,将0.5mol N2和1.5molH2置于密闭的容器中充分反应生成NH3(g),放热19.3kJ, 其热化学方程式为:N2(g) + 3H2(g) 2NH3(g) △H= -38.6kJ·mol-1
2NH3(g) △H= -38.6kJ·mol-1
D.已知25℃、101KPa条件下:4Al(s)+3O2(g)=2A12O3(s) △H=-2834.9 kJ·mol-1,
4Al(s)+2O3(g)=2A12O3(s) △H=-3119.1 kJ·mol-1, 则O2比O3稳定
查看答案和解析>>
科目:高中化学 来源:2015-2016学年辽宁省抚顺市协作校高一下期末化学试卷(解析版) 题型:填空题
甲醇是重要的化工原料。利用合成气(主要成分为CO、CO2和H2)在催化剂的作用下合成甲醇,发生的主要反应如下:
①CO(g)+2H2(g) CH3OH(g) △H1
CH3OH(g) △H1
②CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H2=-58 kJ/mol
CH3OH(g)+H2O(g) △H2=-58 kJ/mol
③CO2(g)+H2(g) CO(g)+H2O(g) △H3=+41 kJ/mol
CO(g)+H2O(g) △H3=+41 kJ/mol
回答下列问题:
(1)CO2的电子式是 。
(2)△H1= kJ/mol,①反应正向的熵变△S 0(填>、<或=)。
(3)在容积为2L的密闭容器中,充入一定量CO2和H2合成甲醇(上述②反应),在其他条件不变时,温度T1、T2对反应的影响图像如图,下列说法正确的是__________(填序号)
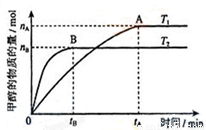
①温度为T1时,从反应到平衡,生成甲醇的平均速率为:v(CH3OH)=nA/tA mol/(L·min)
②当v(CH3OH) = v(H2O)时,说明反应达到平衡
③混合气体的平均相对分子质量A点大于B点
④处于A点的反应体系从T1变到T2,达到平衡时n(H2)与n(CH3OH)比值增大
(4)在T1温度时,将2molCO2和6molH2充入2L密闭容器中,充分反应(上述②反应)达到平衡后,若CO2转化率为50%,,则容器内的压强与起始压强之比为__________;T1温度,反应CH3OH(g)+H2O(g)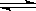 CO2(g)+3H2(g)的平衡常数数值为__________。
CO2(g)+3H2(g)的平衡常数数值为__________。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年辽宁省抚顺市协作校高一下期末化学试卷(解析版) 题型:选择题
a、b、c、d均为短周期元素,a的原子中只有1个电子,b2-和c+离子的电子层结构相同,b与d同主族。下列叙述正确的是
A. a分别与b、c、d形成的二元化合物中a的化合价均为+1
B. b与其他三种元素均可形成至少两种二元化合物
C. a与b形成的化合物中一定只有共价键,b与c形成的化合物中一定只有离子键
D. 原子半径大小顺序d>c>b>a
查看答案和解析>>
科目:高中化学 来源:2015-2016学年广东省肇庆市高二下期末化学试卷(解析版) 题型:选择题
实验测得-25℃时干冰晶体(面心结构)的晶胞边长为acm,其摩尔质量为Mg/mol,则该干冰晶体的密度为(单位:g/cm3)
A.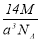 B.
B.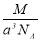 C.
C.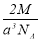 D.
D.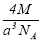
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com