
分析 混合物气体的总物质的量为$\frac{8.96L}{22.4L/mol}$=0.4mol,又因为A与B的物质的量之比为3:1,所以A的物质的量为0.3mol,B的物质的量为0.1mol,设B的相对分子量为x,则A为14x,混合气体的总质量为8.6g,0.3×14x+0.1×x=8.6,得x=2,所以B为H2,A的相对分子质量为28,A可能为CO或N2或C2H4,由此分析解答.
解答 解:混合物气体的总物质的量为$\frac{8.96L}{22.4L/mol}$=0.4mol,又因为A与B的物质的量之比为3:1,所以A的物质的量为0.3mol,B的物质的量为0.1mol,设B的相对分子量为x,则A为14x,混合气体的总质量为8.6g,0.3×14x+0.1×x=8.6,得x=2,所以B为H2,A的相对分子质量为28,A可能为CO或N2或C2H4,
故答案为:CO;N2或C2H4;H2.
点评 本题考查了摩尔质量的简单计算,题目难度中等,要求学生熟练掌握物质的量、摩尔质量间的转化关系.


科目:高中化学 来源: 题型:解答题
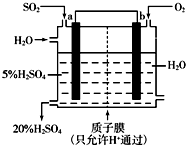 在硫酸工业中,SO2转化为SO3是一个关键步骤
在硫酸工业中,SO2转化为SO3是一个关键步骤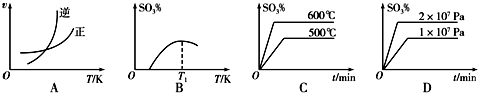
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 过量C02通入氢氧化钙溶液中:CO2+OH-═HCO3- | |
| B. | Na202加入H2180中:2Na2O2+2H218O═4Na++4OH-+18O2↑ | |
| C. | 硅与氢氟酸的反应:Si+4H++4F-═SiF4↑+2H2↑ | |
| D. | 水玻璃中通人过量二氧化碳:Na2SiO3+CO2+H2O═2Na++CO32-+H2SiO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 2015年10月26日,连接上海与杭州的沪杭城际高铁正式开通运营,从上海到杭州只需要45分钟.工业上利用铝热反应焊接钢轨间的缝隙,反应方程式如下:
2015年10月26日,连接上海与杭州的沪杭城际高铁正式开通运营,从上海到杭州只需要45分钟.工业上利用铝热反应焊接钢轨间的缝隙,反应方程式如下:| A. | 氧化剂 | B. | 既是氧化剂又是还原剂 | ||
| C. | 还原剂 | D. | 既不是氧化剂又不是还原剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
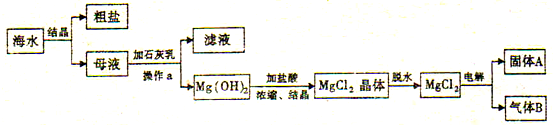
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2SO4→HCl→NaOH→CO2 | B. | Na2SO4→NaCl→NH3•H2O | ||
| C. | NaCl→Na2SO4→NaOH | D. | Na2SO4→NaCl→NaOH |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com