
| A. | v(D)=0.40mol•L-1•s-1 | B. | v(C)=0.50mol•L-1•s_1 | ||
| C. | v(A)=0.30mol•L-1•s-1 | D. | v(B)=0.60mol•L-1•s-1 |
分析 同一可逆反应同一时间段内,各物质的反应速率之比等于其计量数之比,将不同物质的反应速率转化为同一种物质的反应速率,反应速率越大的反应越快,据此解答.
解答 解:同一可逆反应同一时间段内,各物质的反应速率之比等于其计量数之比,将不同物质的反应速率转化为同一种物质的反应速率,反应速率越大的反应越快,将各物质都转化为A物质,
A.v(D)=0.40mol•L-1•s-1,v(A)=0.20mol•L-1•s-1;
B.v(C)=0.50mol•L-1•s-1,v(A)=0.25mol•L-1•s-1;
C.v(A)=0.30mol•L-1•s-1;
D.v(B)=0.60mol•L-1•s-1,v(A)=0.20mol•L-1•s-1;
所以反应速率大小顺序是C>B>A=D,所以反应速率最快的是C,
故选C.
点评 本题考查化学反应速率快慢比较,侧重考查学生分析计算能力,明确化学反应速率与计量数的关系是解本题关键,注意比较时单位要统一.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
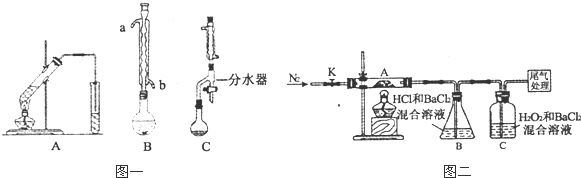
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 全部为Al(OH)3沉淀 | |
| B. | 几乎全部以AlO2-形式存在于溶液中 | |
| C. | 一部分为Al(OH)3沉淀,一部分以Al3+存在于溶液中 | |
| D. | 一部分为Al(OH)3沉淀,一部分以AlO3-形式存在于溶液中 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
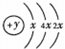 ,B、C可形成离子化合物B3C2,E是同周期元素中原子半径最小的元素.
,B、C可形成离子化合物B3C2,E是同周期元素中原子半径最小的元素. .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| Ⅰ除杂实验 | Ⅱ试剂 | Ⅲ操作方法 | 答案 | ||
| Ⅰ | Ⅱ | Ⅲ | |||
| ①苯(苯酚) | A.饱和Na2CO3溶液 B.NaOH溶液 C.CaO | a.过滤 b.蒸馏 c.分液 | ① | ||
| ②乙醇(水) | ② | ||||
| ③乙酸乙酯(乙酸) | ③ | ||||
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
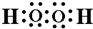 含有的化学键类型有BC(填序号).
含有的化学键类型有BC(填序号). .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1mol C6H14分子中共价键总数为20NA | |
| B. | 1mol乙基(-CH2CH3)电子总数17NA | |
| C. | 常温常压下,26g苯乙烯和苯组成的混合物中所含有的碳原子数为4NA | |
| D. | 标准状况下,22.4L甲醇的分子数中所含羟基数为NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com