
【题目】一定温度下,下列叙述是可逆反应N2(g)+3H2(g)![]() 2NH3(g),在定容密闭容器中达到平衡的标志的是 ( )
2NH3(g),在定容密闭容器中达到平衡的标志的是 ( )
①NH3的生成速率与NH3的分解速率相等;
②单位时间内amolN2生成,同时生成3amolH2;
③N2的浓度不再变化;
④混合气体的总压强不再变化;
⑤混合气体的平均摩尔质量不再变化;
⑥用N2、H2、NH3的物质的量浓度变化表示的反应速率之比为1:3:2;
⑦N2、H2、NH3的分子数目比为1:3:2;
A.②⑤ B.①③④⑤ C.②⑥⑦ D.⑤⑥
【答案】B
【解析】
试题分析:①NH3的生成速率与NH3的分解速率相等,即正逆反应速率相等,达到平衡状态,①正确;②单位时间内amolN2生成,同时生成3amolH2只能说明单方向N2、H2关系,不能说明正逆反应速率的关系,②错误;③N2的浓度不再变化,说明达到了平衡状态,③正确;④因该反应是物质的量在减少的化学反应,物质的量与压强成正比,则混合气体的压强不随时间的变化而变化,达到平衡状态,④正确;⑤混合气体的平均摩尔质量=![]() ,质量是守恒的,物质的量只有达到平衡时才不变,当混合气体的平均摩尔质量不再变化,证明达到了平衡状态,⑤正确;⑥用N2、H2、NH3的物质的量浓度变化表示的反应速率之比为1:3:2是反应进行到任何时刻都成立的关系,不能说明达到了平衡,⑥错误;⑦N2、H2、NH3的分子数目比为1:3:2不是平衡的判据,⑦错误;答案选B。
,质量是守恒的,物质的量只有达到平衡时才不变,当混合气体的平均摩尔质量不再变化,证明达到了平衡状态,⑤正确;⑥用N2、H2、NH3的物质的量浓度变化表示的反应速率之比为1:3:2是反应进行到任何时刻都成立的关系,不能说明达到了平衡,⑥错误;⑦N2、H2、NH3的分子数目比为1:3:2不是平衡的判据,⑦错误;答案选B。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数的值,下列说法正确的是
A. NA个氢氧化铁胶体粒子的质量为107g
B. 0.1 mol·L-1的NaHSO4溶液中,阳离子的数目之和为0.2NA
C. 100g质量分数为17%的H2O2水溶液中含O―O键数目为NA
D. 2.7g铝与足量的稀硫酸和氢氧化钠分别反应,得到氢气的体积在标况下均为3.36L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B两种有机化合物,分子式都为C9H11O2N。
(1)化合物A是天然蛋白质的水解产物,光谱测定显示,分子结构中不存在甲基(—CH3)。化合物A的结构简式是______________。分子结构中不存在甲基,与A互为同分异构体的硝基化合物的结构简式是____________________________________。
(2)化合物B是某种分子式为C9H12的芳香烃一硝化后的唯一产物(硝基连在苯环上)。化合物B的结构简式是______________。与B互为同分异构体的氨基酸的结构简式为___________________________________(氨基在苯环上且苯环上只有两个取代基)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】肼(H2NNH2)是一种高能燃料,有关化学反应的能量变化如下图所示。已知断裂1 mol化学键所需的能量(kJ):N≡N为942、O=O为500、N—N为154,则断裂1 mol N—H键所需的能量(kJ)是:

A. 194 B. 391 C. 516 D. 658
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)短周期元素W、X、Y、Z、M原子序数依次增大,元素W的一种核素的中子数为0,X的原子最外层电子数是次外层的2倍,Z与M同主族,Z2-电子层结构与氖原子相同。
①M在元素周期表中的位置是__________________________。
②化合物p由W、X、Y、M四种元素组成。已知向p溶液中加入FeCl3溶液,溶液变血红色;向p溶液中加入NaOH溶液并加热可放出使湿润的红色石蕊试纸变蓝的气体。p的化学式为_____________。
③(XY)2的性质与Cl2相似,(XY)2与NaOH溶液常温下反应的离子方程式为_____________。
(2)A、B、C、W均为中学常见的纯净物,它们之间有如下转化关系(其它产物及反应条件已略去,反应可以在水溶液中进行):
![]()
Ⅰ. 若A为有刺激性气味的气体,水溶液呈碱性;C为红棕色气体,与水反应生成一元强酸D,D具有强氧化性。
①在催化剂作用下,A与C反应可生成两种无污染物质,该反应化学方程式为________________
②工业上常用Na2CO3溶液吸收C,生成等物质的量的两种钠盐,该反应的离子方程式为_______________
Ⅱ. A、B、C三种物质的溶液均显碱性,焰色反应均为黄色;C常作面包和糕点的发泡剂,受热分解可生成B。
①实验室需配制0.1mol·L-1 A溶液450mL。根据计算用托盘天平称取A的质量为__________ g,在实验中其它操作均正确,若定容时仰视刻度线,则所得溶液浓度________________0.1mol·L-1 (填“大于”“等于”或“小于”)。
②将标准状况下2.24L 的W通入150mL 1mol·L-1的A溶液中,充分反应。总反应的离子方程式为_______________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙烷燃料电池的工作原理示意图如下,下列说法中正确的是

A. a 为负极,电极反应式为 CH3CH3-14e-+18OH-===2CO32-+12H2O
B. 电子从 a 极经导线移向 b 极,再经溶液移向 a 极
C. 电池工作一段时间后电解质溶液的 pH 增大
D. 用该电池电解硫酸铜溶液(电解池的电极为惰性电极),消耗氧气的物质的量与析出铜的物质的量之比为 2∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“低碳循环”引起各国的高度重视,而如何降低大气中CO2的含量及有效地开发利用CO2,引起了全世界的普遍重视。将CO2转化为甲醇:CO2(g)+3H2(g)CH3OH(g)+H2O(g)。
(1)在一恒温恒容密闭容器中充入1 mol CO2和3 mol H2进行上述反应。测得CO2(g)和CH3OH(g)浓度随时间变化如图所示。

①0~10 min内,氢气的平均反应速率为____________,第10 min后,保持温度不变,向该密闭容器中再充入1 mol CO2(g)和1 mol H2O(g),则平衡________(填“正向”“逆向”或“不”)移动。
②若已知:CO2(g)+3H2(g)CH3OH(g)+H2O(g) ΔH=-a kJ·mol-1;
2H2(g)+O2(g)===2H2O(g) ΔH=-b kJ·mol-1;
H2O(g)===H2O(l) ΔH=-c kJ·mol-1;
CH3OH(g)===CH3OH(l) ΔH=-d kJ·mol-1。
则表示CH3OH(l)燃烧热的热化学方程式为______________________________________。
(2)如图,25 ℃时以甲醇燃料电池(电解质溶液为稀硫酸)为电源来电解600 mL一定浓度的NaCl溶液,电池的正极反应式为_________________________________。

在电解一段时间后,NaCl溶液的 pH 变为12(假设电解前后NaCl溶液的体积不变),则理论上消耗甲醇的物质的量为________mol。
(3)向(2)U形管内电解后的溶液(假设NaCl溶液完全被电解)中通入标准状况下89.6 mL 的CO2气体,则所得溶液呈________(填“酸”“碱”或“中”)性,溶液中各离子浓度由大到小的顺序为______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了检验淀粉的水解产物,某学生设计了如下实验方案:
![]()
请回答下列问题
(1)试剂1为20%的H2SO4溶液,其作用是___________________;
(2)试剂2为_____,其作用是____________;
(3)反应①的化学方程式为_______________________;
(4)为了检验淀粉是否已经完全水解,取少量水解液于试管中,加入碘水。则证明淀粉未完全水解的现象是_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
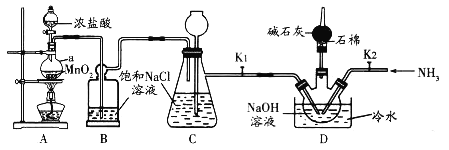
【题目】肼(![]() ,无色液体)是一种用途广泛的化工原料。实验室中先制备次氯酸钠,再用次氯酸钠溶液和氨反应制备肼并验证肼的性质。实验装置如图所示。
,无色液体)是一种用途广泛的化工原料。实验室中先制备次氯酸钠,再用次氯酸钠溶液和氨反应制备肼并验证肼的性质。实验装置如图所示。
已知:![]()
![]() 。当温度超过40℃时,
。当温度超过40℃时,![]() 与
与![]() 溶液反应生成
溶液反应生成![]() 。
。
回答下列问题:
(1)装置B的作用是______________。
(2)为控制D装置中的反应温度,除用冷水浴外,还需采取的实验操作是_________。
(3)当三颈烧瓶中出现黄绿色气体时立即关闭分液漏斗活塞、移去酒精灯、关闭![]() 。此时装置C的作用是_______________。
。此时装置C的作用是_______________。
(4)将D装置水槽中的冷水换为热水,把三颈烧瓶中黄绿色气体赶走后,打开![]() ,通入
,通入![]() ,使其与
,使其与![]() 溶液反应制取肼。理论上通入三颈烧瓶的
溶液反应制取肼。理论上通入三颈烧瓶的![]() 和
和![]() 的最佳物质的量之比为______。
的最佳物质的量之比为______。
(5)请从提供的下列试剂中选择合适试剂,设计合理的实验方案验证肼的还原性(说明操作、现象和结论)。____________。
①淀粉-![]() 溶液 ②稀硫酸(酚酞) ③
溶液 ②稀硫酸(酚酞) ③![]() ④
④![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com