
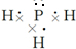 .
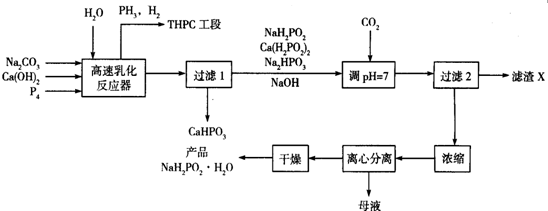
.分析 在高速乳化反应器中加入碳酸钠、氢氧化钙、P4,加入水发生多个反应,其中Ca(OH)2与P4反应生成次磷酸钙及磷化氢,过滤得到CaHPO3,滤液中加入NaH2PO2、Ca(H2PO2)2、Na2HPO3 、NaOH通入CO2调节PH=7,过滤得到滤渣X为碳酸钙,滤液为NaH2PO2,浓缩离心分离、干燥得到NaH2PO2•H2O,母液中除NaH2PO2外,还有的一种主要成分为Na2HPO3,
(1)化合物中元素化合价代数和为0计算得到磷元素的化合价;
(2)高速搅拌的目的是为了加快反应速率;
(3)Ca(OH)2与P4反应生成次磷酸钙及磷化氢依据原子守恒配平书写化学方程式;
(4)流程中通入CO2的目的是将Ca(H2PO2)2转化为NaH2PO2,同时生成碳酸钙沉淀;
(5)依据流程图可知流程中母液中的溶质除NaH2PO2外,还有的一种主要成分为Na2HPO3;
(6)①PH3的电子式书写不能漏掉一对孤对电子对,结构式共用电子对用短线表示;
②含PH3的废气可用NaClO和NaOH的混合溶液处理将其转化为磷酸盐、同时生成氯化钠和水.
解答 解:在高速乳化反应器中加入碳酸钠、氢氧化钙、P4,加入水发生多个反应,其中Ca(OH)2与P4反应生成次磷酸钙及磷化氢,过滤得到CaHPO3,滤液中加入NaH2PO2、Ca(H2PO2)2、Na2HPO3 、NaOH通入CO2调节PH=7,过滤得到滤渣X为碳酸钙,滤液为NaH2PO2,浓缩离心分离、干燥得到NaH2PO2•H2O,母液中除NaH2PO2外,还有的一种主要成分为Na2HPO3,
(1)化合物中元素化合价代数和为0计算得到磷元素的化合价,设磷元素化合价为x价,NaH2PO2•H2O中钠元素化合价+1价,氧元素化合价-2价,氢元素化合价+1价,(+1)+2×(+1)+x+(-2)×2=0,x=+1,
故答案为:+1;
(2)在反应器中加入乳化剂并高速搅拌的目的是为了加快反应速率,
故答案为:加快反应速率;
(3)Ca(OH)2与P4反应生成次磷酸钙及磷化氢,依据原子守恒配平书写化学方程式为:2P4+3Ca(OH)2•6H2O=3Ca(H2PO2)2+2PH3↑,
故答案为:2P4+3Ca(OH)2•6H2O=3Ca(H2PO2)2+2PH3↑;
(4)流程中通入CO2的目的是将Ca(H2PO2)2转化为NaH2PO2,同时生成X为碳酸钙沉淀,
故答案为:将Ca(H2PO2)2转化为NaH2PO2,CaCO3;
(5)依据流程图可知流程中加入了Na2HPO3,所以母液中的溶质除NaH2PO2外,还有的一种主要成分为Na2HPO3,
故答案为:Na2HPO3;
(6)①PH3的电子式书写不能漏掉一对孤对电子,所以电子式为: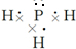 ,
,
故答案为: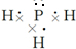 ;
;
②含PH3的废气可用NaClO和NaOH的混合溶液处理将其转化为磷酸盐、同时生成氯化钠和水反应的离子方程式为:PH3+4ClO-+3OH-=PO43-+4Cl-+3H2O,故答案为:PH3+4ClO-+3OH-=PO43-+4Cl-+3H2O.
点评 本题考查了物质制备的方案分析,主要是酸式盐的制备原理和反应产物的判断,注意化学方程式和离子方程式的书写方法,题目难度中等.


 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案 初中学业考试导与练系列答案
初中学业考试导与练系列答案科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 质子数为1.8NA | B. | 分子数为0.1NA | C. | 中子数为2NA | D. | 原子数为2.5NA |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 锥形瓶内溶液颜色变化由黄色变橙色,立即记下滴定管液面所在刻度 | |
| B. | 滴定结束后,滴定管尖嘴处有一悬挂液滴 | |
| C. | 取NaOH溶液时先平视读数,后仰视读数 | |
| D. | 盛NaOH溶液的锥形瓶滴定前用NaOH溶液润洗2次~3次 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
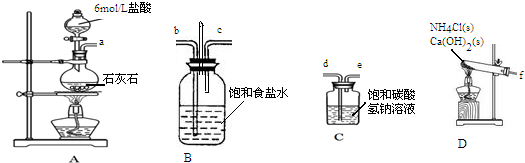 制备碳酸氢钠,然后用碳酸氢钠制备碳酸钠.
制备碳酸氢钠,然后用碳酸氢钠制备碳酸钠.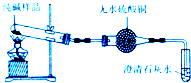
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
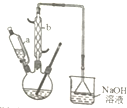 己二酸是合成尼龙-66的主要原料之一.实验室合成己二酸的原理、有关数据及装置示意图如下:
己二酸是合成尼龙-66的主要原料之一.实验室合成己二酸的原理、有关数据及装置示意图如下:
| 物质 | 密度(20℃) | 熔点 | 沸点 | 溶解性 |
| 环己醇 | 0.962g/cm3 | 25.9℃ | 160.8℃ | 20℃时水中溶解度为3.6g,可混溶于乙醇、苯 |
| 己二酸 | 1.360g/cm3 | 152℃ | 337.5℃ | 在水中的溶解度:15℃时1.44g,25℃时2.3g,易溶于乙醇、不溶于苯 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 实验编号 | 锌的状态 | 反应温度/℃ | 收集100mL氢气所需时间/s |
| Ⅰ | 薄片 | 15 | 200 |
| Ⅱ | 薄片 | 25 | 90 |
| Ⅲ | 粉末 | 25 | 10 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
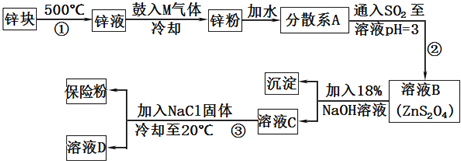
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com