
| 168 |
| 56 |
| 96 |
| 64 |


 ��ҵ����ϵ�д�
��ҵ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��CuO |
| B��Cu��OH��2 |
| C��CuSO4 |
| D��H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

| A���ڢۢݢ� | B���ۢݢߢ� |
| C���ۢܢݢ� | D���ڢۢݢߢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��NO2 |
| B��SO2 |
| C��CO2 |
| D������������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
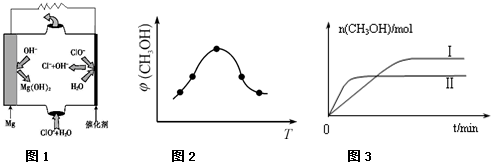
| �� �� | �� | �� |
| ��Ӧ��Ͷ���� | 1molCO2 3molH2 | a molCO2��b molH2�� c molCH3OH��g����c molH2O��g�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A | B | C | |
| ��ʼ���ϣ�mol�� | x | y | z |
A����
| ||
B����
| ||
| C����m+n��p����a��0��������Ӧһ�������Է����� | ||
| D����m+n��p��������Ӧ�������ؼ��ķ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ||
| A��Na2O2�������������ǻ�ԭ�� |
| B��Na2FeO4���������������ǻ�ԭ���� |
| C��3 mol Na2O2������Ӧ����12mol ����ת�� |
| D����Na2FeO4��FeΪ+4�ۣ�����ǿ�����ԣ�������ɱ�� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com