
| A、77.6 kJ |
| B、-77.6 kJ?mol-1 |
| C、+77.6kJ?mol-1 |
| D、-886.8kJ?mol-1 |


科目:高中化学 来源: 题型:
| A、1 mol AlCl3在熔融状态时离子总数为0.4NA |
| B、标准状况下,2.24L苯中含有的C-H键的数目为0.6NA |
| C、2.2g分子式为 2H218O的水中含有的中子数为1.2 NA |
| D、电解饱和食盐水时,当阴极产生H2 22.4L时,电路中转移的电子数为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| 1 |
| 2 |
| 1 |
| 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、PM2.5是指大气中直径接近于2.5×10-6m的颗粒物,也称细颗粒物,这些细颗粒物分散在空气中形成的分散系是胶体 |
| B、将煤气化或液化,获得清洁燃料 |
| C、大力发展新能源汽车,如混合动力汽车、电动汽车等,以减少碳、氮氧化物的排放 |
| D、绿色化学的核心是利用化学原理从头上减少和消除工农业生产等对环境的污染 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
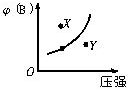 可逆反应mA(s)+nB(g) pC(g)在一定条件下达到平衡后,改变压强,B的体积分数φ(B)与压强的关系如图所示,有关叙述正确的是( )
可逆反应mA(s)+nB(g) pC(g)在一定条件下达到平衡后,改变压强,B的体积分数φ(B)与压强的关系如图所示,有关叙述正确的是( )| A、m+n<p |
| B、n>p |
| C、X点时v(正)>v(逆) |
| D、X点比Y点的正反应速率快 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| t/s | 0 | 2 | 4 | 6 | 8 |
| n(Cl2)/mol | 0 | 0.30 | 0.39 | 0.40 | 0.40 |
| A、保持其他条件不变,升高温度,平衡时c(Cl2)=0.22 mol?L-1,则反应的△H<0 |
| B、若在2 L恒容绝热(与外界没有热量交换)密闭容器进行该反应,化学平衡常数不变 |
| C、保持其他条件不变,起始向容器中充入1.2 molCOCl2、0.20 molCl2和0.20 molCO,反应达到平衡前的速率:υ(正)>υ(逆) |
| D、保持其他条件不变,起始向容器中充入1.0 molCl2和1.2molCO,达到平衡时,Cl2的转化率大于60% |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 用Pt丝灼烧 |
| ① |
| +氯化钡溶液 |
| ② |
| +稀HCl酸化 |
| ③ |
| +稀氨水 |
| ④ |
| +烧碱溶液 |
| ⑤ |
| 吹气 |
| ⑥ |
| A、该无色溶液有可能是明矾溶液 |
| B、这三组实验中,(2)和(3)都是严密合理的 |
| C、步骤④的离子方程式为:Al3++3OH-=Al(OH)3↓ |
| D、步骤⑥的化学方程式可能为:NaAlO2+2H2O+CO2=Al(OH)3↓+NaHCO3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com