

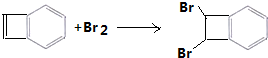
 +2CH3CH2OH$?_{△}^{浓硫酸}$
+2CH3CH2OH$?_{△}^{浓硫酸}$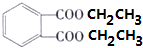 +2H2O
+2H2O分析 根据题给信息知,A被酸性高锰酸钾溶液氧化生成羧酸B,B结构简式为 ,B和D发生酯化反应生成C,结合C分子式知,D结构简式为CH3CH2OH,C结构简式为
,B和D发生酯化反应生成C,结合C分子式知,D结构简式为CH3CH2OH,C结构简式为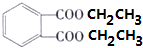 ,再结合题目分析解答.
,再结合题目分析解答.
解答 解:根据题给信息知,A被酸性高锰酸钾溶液氧化生成羧酸B,B结构简式为 ,B和D发生酯化反应生成C,结合C分子式知,D结构简式为CH3CH2OH,C结构简式为
,B和D发生酯化反应生成C,结合C分子式知,D结构简式为CH3CH2OH,C结构简式为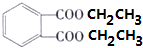 ,
,
(1)根据结构简式知,A的分子式为C8H6,故答案为:C8H6;
(2)A中碳碳双键和溴发生加成反应,所以A能使溴水褪色,反应的化学方程式为 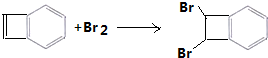 ,故答案为:
,故答案为: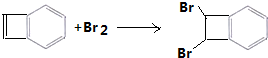 ;
;
(3)反应②为酯化反应,其化学方程式为 +2CH3CH2OH$?_{△}^{浓硫酸}$
+2CH3CH2OH$?_{△}^{浓硫酸}$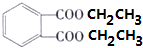 +2H2O,
+2H2O,
故答案为: +2CH3CH2OH$?_{△}^{浓硫酸}$
+2CH3CH2OH$?_{△}^{浓硫酸}$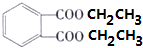 +2H2O;
+2H2O;
(4)B结构简式为 ,1mol羧基能和1mol碳酸氢钠反应生成1mol二氧化碳,所以1molB与足量NaHCO3溶液反应最多产生2molCO2,故答案为:2.
,1mol羧基能和1mol碳酸氢钠反应生成1mol二氧化碳,所以1molB与足量NaHCO3溶液反应最多产生2molCO2,故答案为:2.
点评 本题考查有机物推断,为高频考点,侧重考查学生分析推断及知识综合应用能力,把握官能团及其性质关系是解本题关键,注意结合题给信息进行分析解答,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 向地势低的地方撤离 | |
| B. | 用湿毛巾或蘸有烧碱水的毛巾捂住口鼻撤离 | |
| C. | 观察风向,顺风撤离 | |
| D. | 用湿毛巾或蘸有稀纯碱水的毛巾捂住口鼻撤离 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ,B
,B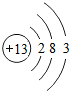 ,二者离子半径:Na+>Al3+(填离子符号).
,二者离子半径:Na+>Al3+(填离子符号).查看答案和解析>>
科目:高中化学 来源: 题型:解答题
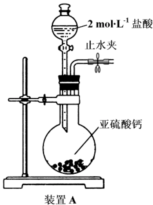


查看答案和解析>>
科目:高中化学 来源: 题型:解答题
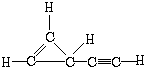 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 温度 | 250℃ | 300℃ | 350℃ |
| K | 2.041 | 0.270 | 0.012 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 某温度时,化学反应速率无论用A、B、C何种物质表示,其数值都是相同的 | |
| B. | 其它条件不变时,升高温度,反应速率加快 | |
| C. | 其它条件不变时,增大压强,反应速率加快 | |
| D. | 若增加或减少A物质的量,反应速率一定会发生明显的变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
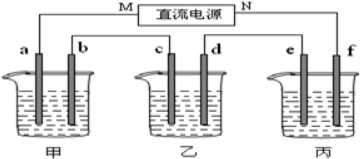
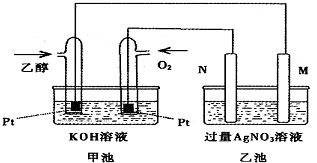 甲乙两池均是电化学装置,按下图连接.乙池中的两个电极分别是石墨电极和铁电极,已知工作过程M、N两个电极的质量均不减少,则下列说法正确的是( )
甲乙两池均是电化学装置,按下图连接.乙池中的两个电极分别是石墨电极和铁电极,已知工作过程M、N两个电极的质量均不减少,则下列说法正确的是( )| A. | M电极的材料是石墨 | |
| B. | 若乙池中某一电极质量增加4.32g时,理论上甲池消耗氧气为224mL | |
| C. | 在此过程中,甲池中OH-向通乙醇的一极移动 | |
| D. | 在此过程中,乙池溶液中电子从M电极向N电极移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com