
| A、2 | B、4 | C、6 | D、8 |
| 28g |
| 0.1mol |


科目:高中化学 来源: 题型:
| A、二氧化硅是生产光纤制品的基本原料 |
| B、水玻璃可用于生产黏合剂和防火剂 |
| C、涂油层、通过电镀加上金属层、制成合金等都是保护金属的措施 |
| D、相同条件下,溶液中Cu2+、Zn2+、H+、Na+的氧化性依次减弱 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、2:3 | B、3:2 |
| C、2:5 | D、1:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、W、X、Y、Z原子的核外最外层电子数的总和为20 |
| B、上述W、X、Y元素的原子半径大小为W<X<Y |
| C、由W与X组成的化合物的沸点总低于由W与Y组成的化合物的沸点 |
| D、W与Y可形成既含极性共价键又含非极性共价键的化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、15g乙烷所含极性共价键的数目为3NA |
| B、0.1mol 甲基含有的质子数6.02NA |
| C、常温下,100mL0.1mol/L醋酸溶液中含醋酸分子为0.01NA |
| D、0.5mol乙醇完全燃烧时,转移的电子数为3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Fe(OH)3溶于氢碘酸:Fe(OH)3+3H+=Fe3++3H2O |
| B、向AlCl3溶液中加入NaAlO2:Al3++3AlO2-+6H2O=4Al (OH)3↓ |
| C、向AlCl3溶液中投入过量的Na:Na+Al3++2H2O=Na++AlO2-+2H2↑ |
| D、氢氧化钙溶液与碳酸氢镁溶液反应:HCO3-+Ca2++OH-=CaCO3↓+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
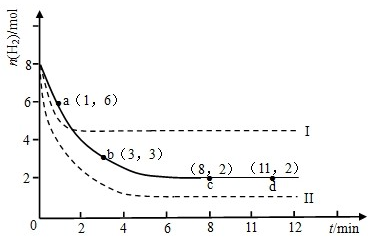 工业上“固定”和利用CO2能有效地减轻“温室’效应.有一种用CO2生产甲醇燃料的方法:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49.0kJ?mol-1
工业上“固定”和利用CO2能有效地减轻“温室’效应.有一种用CO2生产甲醇燃料的方法:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49.0kJ?mol-1查看答案和解析>>
科目:高中化学 来源: 题型:
A、H2(g)+
| ||
| B、H2(g)+O2(g)=2H2O(1)△H=-235kJ.mol-1 | ||
C、H2(g)+
| ||
| D、H2(g)+O2(g)=H2O(1)△H=-470kJ.mol-1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com