
 )可由下列路线合成:
)可由下列路线合成:| HBr/过氧化物 |
| Br2/红磷 |


 ,E在溴、红磷条件下反应得到F,F与苯酚钠反应得到G,结合反应信息Ⅱ可知F为
,E在溴、红磷条件下反应得到F,F与苯酚钠反应得到G,结合反应信息Ⅱ可知F为 ,E为(CH3)2CHCOOH,逆推可得D为(CH3)2CHCHO,C为(CH3)2CHCH2OH,B为(CH3)2CHCH2Br、A为(CH3)2C=CH2,据此解答.
,E为(CH3)2CHCOOH,逆推可得D为(CH3)2CHCHO,C为(CH3)2CHCH2OH,B为(CH3)2CHCH2Br、A为(CH3)2C=CH2,据此解答. ,E在溴、红磷条件下反应得到F,F与苯酚钠反应得到G,结合反应信息Ⅱ可知F为
,E在溴、红磷条件下反应得到F,F与苯酚钠反应得到G,结合反应信息Ⅱ可知F为 ,E为(CH3)2CHCOOH,逆推可得D为(CH3)2CHCHO,C为(CH3)2CHCH2OH,B为(CH3)2CHCH2Br、A为(CH3)2C=CH2,
,E为(CH3)2CHCOOH,逆推可得D为(CH3)2CHCHO,C为(CH3)2CHCH2OH,B为(CH3)2CHCH2Br、A为(CH3)2C=CH2, 反应生成
反应生成 ,属于取代反应,
,属于取代反应, ,其同分异构体符合下列条件:①能使FeCl3溶液显紫色,说明含有酚羟基;②苯环上只有2个取代基,③1mol该物质最多可消耗3mol NaOH,可以确定另外取代基为-OOCCH2CH2CH3或-OOCCH(CH3)2,各有邻、间、对三种位置,故符合条件的同分异构体共有6种,其中核磁共振氢谱为5组峰的为
,其同分异构体符合下列条件:①能使FeCl3溶液显紫色,说明含有酚羟基;②苯环上只有2个取代基,③1mol该物质最多可消耗3mol NaOH,可以确定另外取代基为-OOCCH2CH2CH3或-OOCCH(CH3)2,各有邻、间、对三种位置,故符合条件的同分异构体共有6种,其中核磁共振氢谱为5组峰的为 ,
, ;
; ,故答案为:
,故答案为: .
.


科目:高中化学 来源: 题型:

 | 0 | 10 | 20 | 30 | 40 | 50 |
| NO | 1.00 | 0.68 | 0.50 | 0.50 | 0.60 | 0.60 |
| N2 | 0 | 0.16 | 0.25 | 0.25 | 0.30 | 0.30 |
| CO2 | 0 | 0.16 | 0.25 | 0.25 | 0.30 | 0.30 |
| 温度/℃ | 400 | 500 | 800 |
| 平衡常数K | 9.94 | 9 | 1 |

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、化学键是相邻原子间的相互吸引力 |
| B、离子键是阴、阳离子通过静电作用形成的化学键 |
| C、共价键只存在于共价化合物中 |
| D、非金属元素的原子之间不可能形成离子键 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 室温下,向0.1mol?L-1NaAlO2溶液中逐滴加入0.1mol?L-1稀盐酸,实验测得溶液pH随盐酸体积变化的曲线如图,下列有关说法正确的是( )
室温下,向0.1mol?L-1NaAlO2溶液中逐滴加入0.1mol?L-1稀盐酸,实验测得溶液pH随盐酸体积变化的曲线如图,下列有关说法正确的是( )A、a点时,溶液呈碱性的原因是Al
| ||||
B、a→b段,溶液pH减小,Al
| ||||
| C、b→c段,加入的盐酸主要用于生成Al(OH)3沉淀 | ||||
| D、d点时,Al(OH)3沉淀开始溶解 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、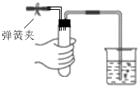 如图装置中,用手捂住试管,烧杯中出现气泡,手放开后,导管中形成一段稳定的水柱 |
B、 如图装置中,向长颈漏斗中加一定量水,并形成水柱,随后水柱下降至瓶中液面相平 |
C、 如图装置中,双手捂住烧瓶,导管中形成一段稳定的水柱,双手放开后,水柱慢慢回落 |
D、 如图装置中,将a管向上提至一段高度,a、b两管之间水面形成稳定的高度差 |
查看答案和解析>>
科目:高中化学 来源: 题型:

| 编号 | 反应物 | 反应前pH | 反应后pH |
| 第1组 | O3+I- | 5.2 | 11.0 |
| 第2组 | O3+I-+Fe2- | 5.2 | 4.1 |
| A、第一组反应pH升高是因为O3氧化I的反应是消耗H+的过程 |
| B、物质A可能是Fe2+ |
| C、Fe2+生成A的过程中,I的转化率显著提高的原因可能是溶液酸性增强,使②、③步骤平衡右移,转化率提高 |
| D、第2组实验18s后,c(I3-)下降的其中一个原因可能是I2(g)的不断生成 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、甲一定是金属单质 |
| B、甲与乙一定含有同种元素 |
| C、丙一定是氧化物 |
| D、该反应一定是氧化还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、人造纤维、合成纤维和光导纤维都是有机高分子化合物 |
| B、钢铁制品和铜制品既能发生吸氧腐蚀又能发生析氢腐蚀 |
| C、明矾用于净水既与盐类的水解有关,又与胶体的性质有关 |
| D、棉花、羊毛及合成纤维完全燃烧都只生成二氧化碳和水 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com