
”¾ĢāÄæ”æŌŚ2 LĆܱÕČŻĘ÷ÖŠ£¬800”ꏱ·“Ó¦2NO£Øg£©£«O2£Øg£©![]() 2NO2£Øg£©ĢåĻµÖŠ£¬n£ØNO£©Ėꏱ¼äµÄ±ä»ÆČē±ķ£ŗ
2NO2£Øg£©ĢåĻµÖŠ£¬n£ØNO£©Ėꏱ¼äµÄ±ä»ÆČē±ķ£ŗ
Ź±¼ä/s | 0 | 1 | 2 | 3 | 4 | 5 |
n£ØNO£©/mol | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
£Ø1£©ÉĻŹö·“Ó¦________£ØĢī”°ŹĒ”±»ņ”°²»ŹĒ”±£©æÉÄę·“Ó¦”£
£Ø2£©ČēĶ¼ĖłŹ¾£¬±ķŹ¾NO2±ä»ÆĒśĻߵďĒ______”£ÓĆO2±ķŹ¾“Ó0”«2sÄŚøĆ·“Ó¦µÄĘ½¾łĖŁĀŹv£½________”£
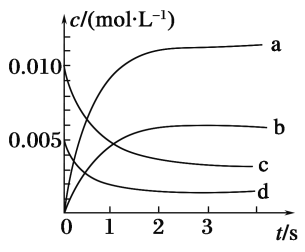
£Ø3£©ÄÜĖµĆ÷øĆ·“Ó¦ŅŃ“ļµ½Ę½ŗāדĢ¬µÄŹĒ________£ØĢīŠņŗÅ£©”£
a£®v£ØNO2£©£½2v£ØO2£©
b£®ČŻĘ÷ÄŚŃ¹Ēæ±£³Ö²»±ä
c£®vÄę£ØNO£©£½2vÕż£ØO2£©
d£®ČŻĘ÷ÄŚĆܶȱ£³Ö²»±ä
”¾“š°ø”æ£Ø1£©ŹĒ””£Ø2£©b””1.5”Į10£3mol”¤£ØL”¤s£©£1””£Ø3£©bc
”¾½āĪö”æ£Ø1£©øĆ·“Ó¦ŹĒæÉÄę·“Ó¦”£
£Ø2£©ÓÉĘ½ŗāĢåĻµ2NO£Øg£©£«O2£Øg£©![]() 2NO2£Øg£©ÖŖ£¬NO2ĪŖÉś³ÉĪļ£¬n£ØNO2£©£½¦¤n£ØNO£©£½0.020mol£0.007mol£½0.013mol
2NO2£Øg£©ÖŖ£¬NO2ĪŖÉś³ÉĪļ£¬n£ØNO2£©£½¦¤n£ØNO£©£½0.020mol£0.007mol£½0.013mol
c£ØNO2£©£½![]() £½0.006 5mol”¤L£1
£½0.006 5mol”¤L£1
¹Ź±ķŹ¾NO2±ä»ÆĒśĻßµÄĪŖb”£
v£ØNO£©£½![]() £½
£½![]() £½
£½![]() £½0.003mol”¤£ØL”¤s£©£1£¬
£½0.003mol”¤£ØL”¤s£©£1£¬
Ōņv£ØO2£©£½![]() v£ØNO£©£½0.001 5mol”¤£ØL”¤s£©£1”£
v£ØNO£©£½0.001 5mol”¤£ØL”¤s£©£1”£
£Ø3£©aĻīÖŠĪ“ÖøĆ÷Õż”¢Äę·“Ó¦ĖŁĀŹ£¬¹ŹĪŽ·ØĖµĆ÷øĆ·“Ó¦ŹĒ·ń“ļµ½Ę½ŗāדĢ¬£»ÓÉÓŚøĆ·“Ó¦ŹĒ·“Ó¦Ē°ŗóĘųĢåĢå»ż²»ĻąµČµÄ·“Ó¦£¬µ±ČŻĘ÷ÄŚŃ¹Ēæ±£³Ö²»±äŹ±£¬ĖµĆ÷øĆ·“Ó¦ŅŃ“ļµ½Ę½ŗāדĢ¬£¬¹ŹbĻīÕżČ·£»cĻīÖŠŅŃĖµĆ÷Õż”¢Äę·“Ó¦ĖŁĀŹĻąµČ£¬¹ŹĖµĆ÷øĆ·“Ó¦ŅŃ“ļµ½Ę½ŗāדĢ¬£»ÓÉÓŚĘųĢå×ÜÖŹĮæ²»±ä£¬ĘųĢå×ÜĢå»żŅ²²»±ä£¬Ņņ“Ė£¬ĪŽĀŪøĆ·“Ó¦ŹĒ·ń“ļµ½Ę½ŗā£¬ČŻĘ÷ÄŚĆܶȱ£³Ö²»±ä£¬¹ŹdĻīĪŽ·ØĖµĆ÷øĆ·“Ó¦ŹĒ·ń“ļµ½Ę½ŗāדĢ¬”£


 ×Ö“Ź¾ä¶ĪĘŖĻµĮŠ“š°ø
×Ö“Ź¾ä¶ĪĘŖĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æÄܹ»æģĖŁ”¢Ī¢Į攢¾«Č·µÄ²ā¶ØĻą¶Ō·Ö×ÓÖŹĮæµÄĪļĄķ·½·ØŹĒ £Ø £©
A. ÖŹĘ× B. ŗģĶā¹āĘ× C. ×ĻĶā¹āĘ× D. ŗĖ“Ź²ÕńĘ×
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŅŃÖŖ“æĖ®ÄÜ·¢ÉśĪ¢ČõµÄµēĄė£¬ĘäµēĄė·½³ĢŹ½æɱķŹ¾ĪŖ£ŗ2H2O![]() H3O++OH££ØH3O+Ķس£¼ņŠ“ĪŖH+£©”£
H3O++OH££ØH3O+Ķس£¼ņŠ“ĪŖH+£©”£
ŌŚĖ®ÖŠ·¢ÉśµÄ·“Ó¦¾ŁĄż£ŗ
NaOH+HCl==NaCl+H2O£¬
Na2O+2HCl==2NaCl+H2Oӣ
£Ø1£©ŅŗĢ¬°±(NH3)Óė“æĖ®ĻąĖĘ£¬ĘäµēĄė·½³ĢŹ½æɱķŹ¾ĪŖ_________________”£
£Ø2£©Š“³öĻĀĮŠĪļÖŹŌŚŅŗĢ¬°±ÖŠ·¢Éś·“Ó¦µÄ»Æѧ·½³ĢŹ½£ŗ
¢ŁNaNH2+NH4Cl”Ŗ_______________£»
¢ŚK3N+(NH4)2SO4”Ŗ_____________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ£Ø £©
A.½öÓĆĖįŠŌøßĆĢĖį¼ŲČÜŅŗæÉĒų·Ö±½ŗĶ¼×±½
B.½öÓĆĀČ»ÆĢśČÜŅŗæÉĒų·Ö±½·ÓĻ”ČÜŅŗŗĶøŹÓĶ
C.½öÓĆĻõĖįŗĶĻõĖįŅųČÜŅŗæÉŃéÖ¤Ā±“śĢžÖŠĀ±Ō×ÓµÄÖÖĄą
D.½öÓĆäåµÄĖÄĀČ»ÆĢ¼ČÜŅŗæÉĒų±šŅŗĢ¬µÄÖ²ĪļÓĶŗĶ¶ÆĪļÓĶ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ½öøıäĻĀĮŠŅ»øöĢõ¼ž£¬ĶعżĢįøß»ī»Æ·Ö×ӵİŁ·ÖŹżĄ“Ģįøß·“Ó¦ĖŁĀŹµÄŹĒ
A. ½µµĶĪĀ¶ČB. Ōö“óŃ¹Ēæ
C. ¼Ó“߻ƼĮD. ¼Ó“ó·“Ó¦ĪļÅضČ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠĪļÖŹÖŠ£¬ŹōÓŚµē½āÖŹµÄŹĒ£Ø””””£©
A.CO2
B.H2
C.Na2SO4
D.Cu
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ²ŻĖįīÜæÉÓĆÓŚÖøŹ¾¼ĮŗĶ“߻ƼĮµÄÖʱø”£ÓĆĖ®īÜæó£ØÖ÷ŅŖ³É·ÖĪŖCo2O3£¬ŗ¬ÉŁĮæFe2O3”¢A12O3”¢MnO”¢MgO”¢CaO”¢SiO2µČ£©ÖĘČ”CoC2O4”¤2H2O¹¤ŅÕĮ÷³ĢČēĻĀ£ŗ

ŅŃÖŖ£ŗ¢Ł½ž³öŅŗŗ¬ÓŠµÄŃōĄė×ÓÖ÷ŅŖÓŠH+”¢Co2+”¢Fe2+”¢Mn2+”¢Ca2+”¢Mg2+”¢Al3+µČ£»
¢ŚĖįŠŌĢõ¼žĻĀ£¬ClO3-²»»įŃõ»ÆCo2+£¬ClO3-×Ŗ»ÆĪŖCl-£»
¢Ū²æ·ÖŃōĄė×ÓŅŌĒāŃõ»ÆĪļŠĪŹ½³ĮµķŹ±ČÜŅŗµÄpH¼ū±ķ£ŗ
³ĮµķĪļ | Fe(OH)3 | Al(OH)3 | Co(OH)2 | Fe(OH)2 | Mn(OH)2 |
ĶźČ«³ĮµķµÄpH | 3.7 | 5.2 | 9.2 | 9.6 | 9.8 |
£Ø1£©½ž³ö¹ż³ĢÖŠ¼ÓČėNa2SO3µÄÖ÷ŅŖÄæµÄŹĒ________”£
£Ø2£©Ļņ½ž³öŅŗÖŠ¼ÓČėNaClO3µÄĄė×Ó·“Ó¦·½³ĢŹ½£ŗ_________”£
£Ø3£©ŅŃÖŖ£ŗ³£ĪĀĻĀNH3”¤H2O![]() NH4+£«OH- Kb£½1.8”Į10-5
NH4+£«OH- Kb£½1.8”Į10-5
H2C2O4![]() H+£«HC2O4- Ka1£½5.4”Į10-2
H+£«HC2O4- Ka1£½5.4”Į10-2
HC2O4-![]() H£«C2O42- Ka2£½5.4”Į10-5
H£«C2O42- Ka2£½5.4”Į10-5
ŌņøĆĮ÷³ĢÖŠĖłÓĆ(NH4)2C2O4ČÜŅŗµÄpH______7£ØĢī”°£¾”±»ņ”°£¼”±»ņ”°=”±£©”£
£Ø4£©¼ÓČė(NH4)2C2O4 ČÜŅŗŗóĪö³ö¾§Ģ壬ŌŁ¹żĀĖ”¢Ļ“µÓ£¬Ļ“µÓŹ±æÉŃ”ÓƵďŌ¼ĮÓŠ£ŗ________”£
A£®ÕōĮóĖ® B£®×ŌĄ“Ė® C£®±„ŗĶµÄ(NH4)2C2O4ČÜŅŗ D£®Ļ”ŃĪĖį
£Ø5£©ŻĶČ”¼Į¶Ō½šŹōĄė×ӵįĶČ”ĀŹÓėpHµÄ¹ŲĻµČēÓŅĶ¼1£¬ŻĶČ”¼ĮµÄ×÷ÓĆŹĒ________£»ĘäŹ¹ÓƵďŹŅĖpH·¶Ī§ŹĒ________”£
A£®2.0”«2.5 B£®3.0”«3.5 C£®4.0”«4.5
£Ø6£©CoC2O4”¤2H2OČČ·Ö½āÖŹĮæ±ä»Æ¹ż³ĢČēĶ¼2ĖłŹ¾”£ĘäÖŠ600”ęŅŌĒ°ŹĒøō¾ųæÕĘų¼ÓČČ£¬600 ”ęŅŌŗóŹĒŌŚæÕĘųÖŠ¼ÓČČ”£A”¢B”¢C¾łĪŖ“æ¾»Īļ£»CµćĖłŹ¾²śĪļµÄ»ÆѧŹ½ŹĒ________”£
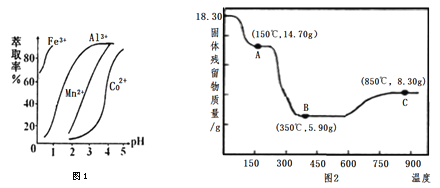
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”潫30 mL 0.5 mol”¤L£1µÄNaClČÜŅŗ¼ÓĖ®Ļ”ŹĶµ½500 mL£¬Ļ”ŹĶŗóČÜŅŗÖŠNaClµÄĪļÖŹµÄĮæÅضČĪŖ£Ø £©
A£®0.03 mol”¤L£1 B£®0.3 mol”¤L£1
C£®0.05 mol”¤L£1 D£®0.04 mol”¤L£1
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æµ±¹āŹųĶعżĻĀĮŠ·ÖÉ¢Ļµ£ŗ¢Ł³¾°£µÄæÕĘų ¢ŚĻ”ĮņĖį ¢ŪÕōĮóĖ® ¢ÜÄ«Ė®£¬ÄܹŪ²ģµ½ÓŠ¶”“ļ¶ūĻÖĻóµÄŹĒ£Ø””””£©
A.¢Ł¢Ś
B.¢Ś¢Ū
C.¢Ł¢Ü
D.¢Ś¢Ü
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com