
MgH2O2电池可用于驱动无人驾驶的潜航器。该电池以海水为电解质溶液,示意图如右。该电池工作时,下列说法正确的是 ( )

A.Mg电极是该电池的正极
B.H2O2在石墨电极上发生氧化反应
C.石墨电极附近溶液的pH增大
D.溶液中Cl-向正极移动
 考前必练系列答案
考前必练系列答案科目:高中化学 来源: 题型:
用NA表示阿伏加德罗常数的值。下列叙述正确的是
A.18 g的D216O中含有的中子数为9 NA
B.物质的量浓度均为1.0mol/L的硫酸与高氯酸(HClO4)溶液中含有的氧原子数均为4NA
C.33.6 L NO2溶于足量的水得到的溶液中含有的NO数为NA
D.32 g铜发生氧化还原反应,一定失去NA个电子
查看答案和解析>>
科目:高中化学 来源: 题型:
二甲醚(CH3OCH3)和甲醇(CH3OH)被称为21世纪的新型燃料。以CH4和
H2O为原料制备二甲醚和甲醇的工业流程如下:

请填空:
(1)一定条件下,反应室1中发生反应CH4(g)+H2O(g) CO(g)+3H2(g) ΔH>0。
CO(g)+3H2(g) ΔH>0。
其它条件不变,只降低温度,逆反应速率将 (填“增大”、“减小”或“不变”)。
 (2)反应室3(容积可变的密闭容器)中 0.2molCO与
(2)反应室3(容积可变的密闭容器)中 0.2molCO与
0.4molH2在催化剂作用下发生可逆反应生成甲醇:
CO(g)+2H2(g) CH3OH(g),CO的平衡转化率
CH3OH(g),CO的平衡转化率
与温度、压强的关系如右图所示,则:
①P1 P2 (填“<”、“>”或“=”)。
②在压强P1下,100℃时反应达到化学平衡,反应室3的容积变为2L,此时 若温度不变,再加入1.0molCO后重新达到平衡,CO的平衡转化率 (填“增大”、“不变”或“减小”)。
③保持容积为2L不变,温度100℃不变,向反应室3中再通入0.2molCO与0.4molH2, CO的平衡转化率 (填“增大”、“不变”或“减小”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
一种碳纳米管能够吸附氢气,可作二次电池(如下图所示)的碳电极。该电池的电解质溶液为6 mol·L-1的KOH溶液,下列说法正确的是 ( )

A.充电时阴极发生氧化反应
B.充电时将碳电极与电源的正极相连
C.放电时碳电极反应为H2-2e-===2H+
D.放电时镍电极反应为NiO(OH)+H2O+e-===Ni(OH)2+OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
已知在酸性条件下发生的反应为AsO +2I-+2H+===AsO
+2I-+2H+===AsO +I2+H2O,在碱性条件下发生的反应为AsO
+I2+H2O,在碱性条件下发生的反应为AsO +I2+2OH-===AsO
+I2+2OH-===AsO +H2O+2I-。设计如图装置(C1、C2均为石墨电极),分别进行下述操作:
+H2O+2I-。设计如图装置(C1、C2均为石墨电极),分别进行下述操作:

Ⅰ.向B烧杯中逐滴加入浓盐酸
Ⅱ.向B烧杯中逐滴加入40% NaOH溶液
结果发现检流计指针均发生偏转。
试回答下列问题:
(1)两次操作中指针为什么发生偏转?
(2)两次操作过程中指针偏转方向为什么相反?试用化学平衡移动原理解释之。
(3)操作Ⅰ过程中C1棒上发生的反应为______________________________________;
(4)操作Ⅱ过程中C2棒上发生的反应为______________________________________。
(5)操作Ⅱ过程中,盐桥中的K+移向______烧杯溶液(填“A”或“B”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)[2012·海南,13(4)]肼—空气燃料电池是一种碱性电池,该电池放电时,负极的反应式为 ________________________________________________________________。
(2)[2012·江苏,20(3)]铝电池性能优越,AlAgO电池可用作水下动力电源,其原理如图所示。该电池反应的化学方程式为_________________________________________。

查看答案和解析>>
科目:高中化学 来源: 题型:
一种太阳能电池的工作原理如下图所示,电解质为铁氰化钾K3[Fe(CN)6]和亚铁氰化钾K4[Fe(CN)6]的混合溶液,下列说法不正确的是 ( )

A.K+移向催化剂b
B.催化剂a表面发生的化学反应:[Fe(CN)6]4--e-===[Fe(CN)6]3-
C.[Fe(CN)6]3-在催化剂b表面被氧化
D.电解池溶液中的[Fe(CN)6]4-和[Fe(CN)6]3-浓度基本保持不变
查看答案和解析>>
科目:高中化学 来源: 题型:
在2A(g)+B(g) 3C(g)+4D(g)反应中,表示该反应速率最快的是
3C(g)+4D(g)反应中,表示该反应速率最快的是
A.v(A )=0.5 mol·L-1·s-1 B.v(B)=0.5 mol·L-1·s-1
)=0.5 mol·L-1·s-1 B.v(B)=0.5 mol·L-1·s-1
C.v(C)=1.8 mol·L-1·min-1 D.v(D)=1 mol·L-1·s-1
查看答案和解析>>
科目:高中化学 来源: 题型:
请回答以下问题:
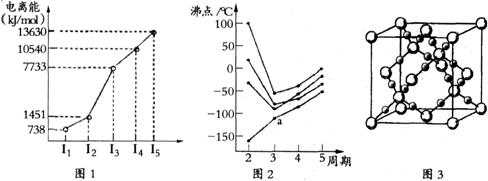
(1)第四周期的某主族元素,其第一至五电离能数据如下图1所示,则该元素对应原子的M层电子排布式为 。
(2)如下图2所示,每条折线表示周期表ⅣA-ⅦA中的某一族元素氢化物的沸点变化。每个小黑点代表一种氢化物,其中a点代表的是 。简述你的判断依据
。
(3)CO2在高温高压下所形成的晶体其晶胞如下图3所示.该晶体的类型属于 (选填“分子”“原子”“离子”或“金属”)晶体。
(4)BCl3原子的杂化方式为 。第一电离能介于B、N之间的第二周期元素有
种。写出与BCl3结构相同的一种等电子体(写离子) 。
|
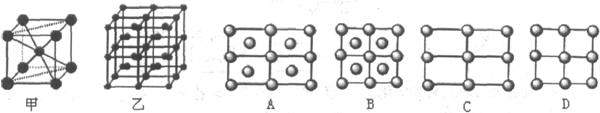
D的醋酸盐晶体局部结构如图,该晶体中含有的化学键
是________ (填选项序号)。
①极性键 ②非极性键 ③配位键 ④金属键
(6)Fe的一种晶体如甲、乙所示,若按甲虚线方向切乙得到的A-D图中正确的是 .铁原子的配位数是 ,假设铁原子的半径是r cm,该晶体的密度是p g/cm3,则铁的相对原子质量为 (设阿伏加德罗常数的值为NA)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com