
分析 AlCl3为强酸弱碱盐,铝离子水解导致溶液呈酸性;将AlCl3溶液蒸干过程中,氯化铝水解生成HCl和Al(OH)3,温度越高HCl挥发性越强,导致蒸干时得到的固体是Al(OH)3,灼烧Al(OH)3得到的固体是氧化铝;Al3+与HCO3-发生双水解.
解答 解:AlCl3为强酸弱碱盐,铝离子水解导致溶液呈酸性,水解方程式为Al3++3H2O?Al(OH)3+3H+;将AlCl3溶液蒸干过程中,氯化铝水解生成HCl和Al(OH)3,温度越高HCl挥发性越强,导致蒸干时得到的固体是Al(OH)3,灼烧Al(OH)3得到的固体是氧化铝,方程式为2Al(OH)3$\frac{\underline{\;\;△\;\;}}{\;}$Al2O3+3H2O;Al3+与HCO3-发生双水解生成氢氧化铝沉淀和二氧化碳气体,离子方程式为:Al3++3HCO3-=Al(OH)3+3CO2↑.
故答案为:酸;Al3++3H2O?Al(OH)3+3H+;Al2O3;2Al(OH)3$\frac{\underline{\;\;△\;\;}}{\;}$Al2O3+3H2O.
点评 本题考查盐类水解,根据形成盐的酸、碱强弱确定盐的类型,从而确定溶液酸碱性,注意:蒸干、灼烧难挥发性酸的盐时得到盐本身,蒸干、灼烧挥发性酸的盐时得到金属氧化物.


科目:高中化学 来源: 题型:推断题
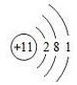 .
.查看答案和解析>>
科目:高中化学 来源: 题型:实验题
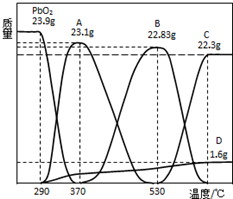 某种铅酸蓄电池具有廉价、长寿命、大容量的特点,它使用的电解质是可溶性的甲基磺酸铅,电池的工作原理:Pb(s)+PbO2(s)+2H2SO4(aq)$?_{充电}^{放电}$2PbSO4(s)+2H2O(l)
某种铅酸蓄电池具有廉价、长寿命、大容量的特点,它使用的电解质是可溶性的甲基磺酸铅,电池的工作原理:Pb(s)+PbO2(s)+2H2SO4(aq)$?_{充电}^{放电}$2PbSO4(s)+2H2O(l)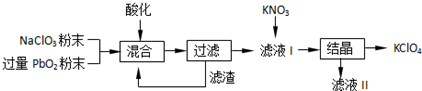
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
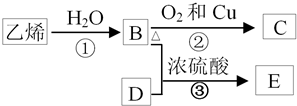
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
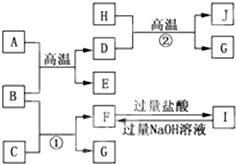 如图A~J均代表无机物或其水溶液,其中B、D、G是单质,B是地壳中含量最高的金属元素,G是气体,J是磁性材料,常温下H为无色液体.
如图A~J均代表无机物或其水溶液,其中B、D、G是单质,B是地壳中含量最高的金属元素,G是气体,J是磁性材料,常温下H为无色液体.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com