
| 物质 | H2(g) | O2(g) | H2O(g) |
| 1mol分子中的化学键断裂时需要吸收的能量/KJ | 436 | 496 | a |
| A. | 463 | B. | 260 | C. | 926 | D. | 970 |
分析 根据盖斯定律计算反应2H2(g)+O2(g)=2H2O(l)的△H,结合反应热等于反应物的总键能减生成物的总键能列方程计算.
解答 解:在25℃、1.013×105Pa条件下,1molH2在氧气中完全燃烧后放出286KJ热量,即热化学方程式为2H2(g)+O2(g)=2H2O(l)△H=-286×2kJ/mol,又1mol水蒸气转化为液态水放出热量为44KJ,所以2H2(g)+O2(g)=2H2O(g)△H=-286×2+88=-484kJ/mol,反应热等于反应物的总键能减生成物的总键能,则-484=2×436+496-2a,a=926,
故选C.
点评 本题考查反应热的计算,题目难度不大,注意反应热与键能的计算关系以及物质的不同聚集状态的转化.


 励耘书业暑假衔接宁波出版社系列答案
励耘书业暑假衔接宁波出版社系列答案科目:高中化学 来源: 题型:选择题
| A. | CH4+Cl2$\stackrel{光照}{→}$CH2Cl+HCl | B. | 2Cl2+2Ca(OH)2═CaCl2+Ca(ClO)2+2H2O | ||
| C. | CH2=CH2+Br2$\stackrel{一定条件}{→}$CH2BrCH2Br | D. | 3NO2+H2O═2HNO3+NO |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Al(OH)3 |
| 开始沉淀 | 2.3 | 7.5 | 3.4 |
| 完全沉淀 | 3.2 | 9.7 | 4.4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2→H+H | B. | H+Cl→HCl | ||
| C. | C(石墨)→C(金刚石) | D. | CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH2=CH2+H2$\stackrel{催化剂}{→}$C2H6 | |
| B. | 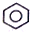 +HNO3$→_{55-60℃}^{浓H_{2}SO_{4}}$ +HNO3$→_{55-60℃}^{浓H_{2}SO_{4}}$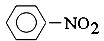 +H2O +H2O | |
| C. | CH3COOCH2CH3+H2O$→_{△}^{稀H_{2}SO_{4}}$CH3COOH+CH3CH2OH | |
| D. | CH4+Cl2$\stackrel{光照}{→}$CH3Cl+HCl |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ⑪
⑪ ⑫
⑫
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烯能与高锰酸钾发生取代反应而使酸性高锰酸钾溶液褪色 | |
| B. | 苯能与高锰酸钾发生取代反应而使酸性高锰酸钾溶液褪色 | |
| C. | 乙烯能与溴单质发生加成反应而使溴水褪色 | |
| D. | 苯能与溴单质发生加成反应而使溴水褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 不-定存在K+ | B. | 100mL溶液中含有0.02molCO32- | ||
| C. | 可能存在Cl- | D. | 一定不存在Mg2+ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com