


分析 Ⅰ.(1)依据热化学方程式和盖斯定律计算所需化学方程式,反应的焓变与化学计量数成正比;
Ⅱ.(2)氯化水解法产物是三氯氧磷和盐酸,结合原子守恒分析;
(3)根据化合价规则计算元素的化合价,在化合物中正负化合价代数和为零;
(4)在沉淀前先加入适量漂白粉使废水中的H3PO3氧化为PO43-,加入生石灰后能完全转化为磷酸的钙盐,达到较高的回收率;
Ⅲ.(5)根据图1、2分析磷的沉淀回收率;
(6)NaH2PO4溶液中存在水解平衡:H2PO4-+H2O?H3PO4+OH-,电离平衡:H2PO4-?HPO42-+H+,电离常数K1>K2>K3,H2PO4-在水溶液里电离程度大于水解程度.
解答 解:Ⅰ.(1)①2Ca3(PO4)2(s)+5C(s)=6CaO(s)+P4(s)+5CO2(g)△H1=+Ql kJ•mol-1
②CaO(s)+SiO2(s)=CaSiO3(s)△H2=-Q2 kJ•mol-1
依据热化学方程式和盖斯定律计算得到①-②×6得到化学方程式为:2Ca3(PO4)2(s)+6SiO2(s)+5C(s)$\frac{\underline{\;高温\;}}{\;}$6CaSiO3(s)+P4(s)+5CO2(g))△H=(Ql-6Q2 )kJ•mol-1,
故答案为:2Ca3(PO4)2(s)+6SiO2(s)+5C(s)$\frac{\underline{\;高温\;}}{\;}$6CaSiO3(s)+P4(s)+5CO2(g))△H=(Ql-6Q2 )kJ•mol-1;
Ⅱ.(2)氯化水解法是用三氯化磷、氯气与水反应生成三氯氧磷和盐酸,其化学方程式为:PCl3+H2O+Cl2=POCl3+2HCl,
故答案为:PCl3+H2O+Cl2=POCl3+2HCl;
(3)氯元素显-1价,氢元素显+1价,氧元素显-2价,设磷元素的化合价是x,根据在化合物中正负化合价代数和为零,可得:POCl3、H3PO4、H3PO3中磷元素的化合价分别为+5、+5、+3,
故答案为:+5、+5、+3;
(4)氯化水解法生产三氯氧磷会产生含磷(主要为H3PO4、H3PO3等)废水,在废水中先加入适量漂白粉,使废水中的H3PO3氧化为PO43-,使其加入生石灰后能完全转化为磷酸的钙盐,达到较高的回收率;
故答案为:将+3价的磷氧化为+5价的磷(将H3PO3氧化为H3PO4);
Ⅲ.(5)根据图1、2可确定pH=10、反应时间30 min时磷的沉淀回收率较高,则处理该厂废水最合适的工艺条件为pH=10、反应时间30 min,
故答案为:bc;
(6)NaH2PO4溶液中存在水解平衡:H2PO4-+H2O?H3PO4+OH-,电离平衡:H2PO4-?HPO42-+H+;磷酸是三元酸,其各级电离常数如下:K1=7.1×10-3 K2=6.3×l0-8 K3=4.2×10-13,K1>K2>K3,H2PO4-在水溶液里电离程度大于水解程度,0.1mol/L的NaH2PO4溶液中按三级电离全部电离2CK3<K2,所以NaH2PO4溶液中按二级电离粗略计算,0.1mol/L>6.3×l0-8 ,所以溶液的pH=-lgc(H+)≈1,实际略小于1,显酸性,即PH<7,
故答案为:<.
点评 本题考查了物质的制备方案设计,题目涉及热化学方程式的书写、氧化还原的应用、化合价的计算、PH的应用等,题目综合性较强,难度中等,侧重于考查学生的分析能力和对基础知识的综合应用能力.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:解答题
 一定条件下,在某密闭恒压容器中发生反应:2M(g)?N(g)△H=a kJ•mol-1,达到平衡时,N的质量分数[ω(N)]与温度的变化关系如图所示:
一定条件下,在某密闭恒压容器中发生反应:2M(g)?N(g)△H=a kJ•mol-1,达到平衡时,N的质量分数[ω(N)]与温度的变化关系如图所示:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烯与氯气加成(1,2-二氯乙烷) | |
| B. | 乙炔先加一分子HCl,再加H2(氯乙烷) | |
| C. | Cl2和苯用FeCl3作催化剂(氯苯) | |
| D. | 等物质的量的Cl2和C2H6在光照条件下(氯乙烷) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 离子 | Cu2+ | Fe2+ | Mg2+ |
| pH | 5.2 | 7.6 | 10.4 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 元素编号 | 元素性质与原子(或分子)结构 |
| T | 最外层电子数是次外层电子数的3倍 |
| X | 常温下单质分子为双原子分子,分子中含有3对共用电子对 |
| Y | M层比K层少1个电子 |
| Z | 第三周期元素的金属离子中半径最小 |
 .
.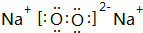 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 把分别盛有甲、乙、丙气体的试管到插入盛有水的烧杯中,一段时间后,观察到如图所示的现象,对甲、乙、丙气体的分析正确的是( )
把分别盛有甲、乙、丙气体的试管到插入盛有水的烧杯中,一段时间后,观察到如图所示的现象,对甲、乙、丙气体的分析正确的是( )| A. | 甲、乙、丙气体都易溶于水 | B. | 乙气体比甲气体更易溶于水 | ||
| C. | 可以采用排水集气方法收集丙气体 | D. | 不可以用排空气法收集甲气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ | ⑩ |
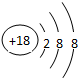 .元素⑩名称为溴单质与水反应化学方程式Br2+H2O=HBr+HBrO.
.元素⑩名称为溴单质与水反应化学方程式Br2+H2O=HBr+HBrO.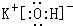 .
.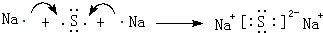 ,该化合物属于离子(填“共价”或“离子”)化合物.
,该化合物属于离子(填“共价”或“离子”)化合物.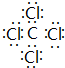 、
、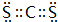 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com