
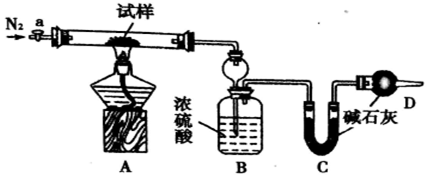
分析 A装置中加热药品时发生反应2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O、Na2CO3•10H2O$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+10H2O,生成的水蒸气被浓硫酸吸收,C中碱石灰吸收碳酸氢钠分解生成的二氧化碳,D干燥空气;
(1)加热条件下,碳酸氢钠分解生成碳酸钠、二氧化碳和水,十水碳酸钠分解生成碳酸钠和水;
(2)浓硫酸具有吸水性;碱石灰具有吸水性和吸收酸性气体的性质;
(3)通入的氮气能把装置中的CO2和水蒸气排出;
(4)实验结束后发现装置A中硬质玻璃管右端有水珠,可以利用二氧化碳质量计算,利用实验中所提供的数据得到准确的w(NaHCO3).
解答 解:A装置中加热药品时发生反应2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O、Na2CO3•10H2O$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+10H2O,生成的水蒸气被浓硫酸吸收,C中碱石灰吸收碳酸氢钠分解生成的二氧化碳,D干燥空气;
(1)加热条件下,碳酸氢钠分解生成碳酸钠、二氧化碳和水,十水碳酸钠分解生成碳酸钠和水,反应方程式分别为2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O、Na2CO3•10H2O$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+10H2O,
故答案为:2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O;Na2CO3•10H2O$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+10H2O;
(2)浓硫酸具有吸水性,所以B作用是吸收反应生成的水蒸气;碱石灰具有吸水性和吸收酸性气体的性质,所以C装置的作用是吸收反应生成的二氧化碳,
故答案为:吸收反应生成的水蒸气;吸收反应生成的二氧化碳;
(3)通入的氮气能把装置中的CO2和水蒸气排出,使这两种气体完全被吸收,从而计算碳酸氢钠样品含量,
故答案为:把装置中的CO2和水蒸气排出被装置B和装置C完全吸收;
(4)实验结束后发现装置A中硬质玻璃管右端有水珠,可以利用二氧化碳质量计算,利用实验中所提供的数据得到准确的w(NaHCO3)=$\frac{\frac{{m}_{5}-{m}_{3}}{44}×84}{11{m}_{1}}$×100%=$\frac{42({m}_{5}-{m}_{3})}{11{m}_{1}}$×100%;
故答案为:$\frac{42({m}_{5}-{m}_{3})}{11{m}_{1}}$×100%.
点评 本题考查物质含量测定,为高频考点,侧重考查学生实验操作、实验分析和评价、计算能力,明确实验原理、实验操作规范是解本题关键,知道各个仪器作用,题目难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
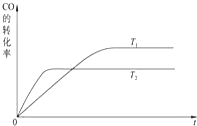 甲醇是一种可再生能源,具有广泛的开发和应用前景.工业上一般可采用如下反应来合成甲醇:CO(g)+2H2(g)?CH3OH(g)△H=-a kJ/mol. 在T℃时,往一个体积固定为1L的密闭容器中加入1mol CO和2mol H2,反应达到平衡时,容器内的压强是开始时的3/5.
甲醇是一种可再生能源,具有广泛的开发和应用前景.工业上一般可采用如下反应来合成甲醇:CO(g)+2H2(g)?CH3OH(g)△H=-a kJ/mol. 在T℃时,往一个体积固定为1L的密闭容器中加入1mol CO和2mol H2,反应达到平衡时,容器内的压强是开始时的3/5.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
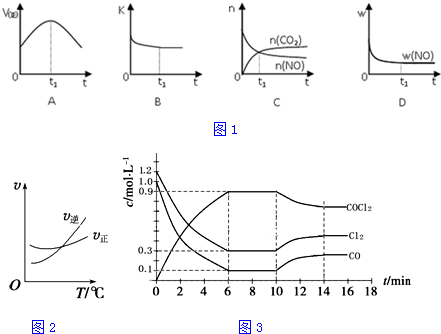
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 序号 | c(ClNO)/mol•L-1 | v/mol•L-1•s-1 |
| ① | 0.30 | 3.6×10-8 |
| ② | 0.60 | 1.44×10-7 |
| ③ | 0.90 | 3.24×10-7 |
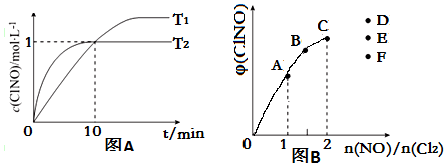
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | “霾尘积聚难见路人”,雾霾所形成的气溶胶有丁达尔效应 | |
| B. | “熬胆矾铁釜,久之亦化为铜”,该过程发生了置换反应 | |
| C. | “青蒿一握,以水二升渍,绞取汁”,屠呦呦对青蒿素的提取属于化学变化 | |
| D. | 大气中二氧化碳含量的增多是造成“温室效应”的主要原因 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
 实验室配制500mL 0.2mol/L的FeSO4溶液,实验操作步骤有:
实验室配制500mL 0.2mol/L的FeSO4溶液,实验操作步骤有:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com