
| A£® | 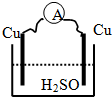 | B£® | 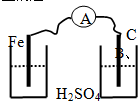 | C£® | 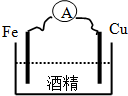 | D£® | 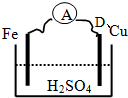 |
·ÖĪö ¹¹³ÉŌµē³ŲŠč¾ß±øŅŌĻĀĢõ¼ž£ŗĮ½øö»īĘĆŠŌ²»Ķ¬µÄµē¼«£¬µē½āÖŹČÜŅŗ£¬ŠĪ³É±ÕŗĻ»ŲĀ·£¬“ęŌŚÄÜ×Ō¶Æ·¢ÉśµÄŃõ»Æ»¹Ō·“Ó¦£¬ŅŌ“ĖĄ“½ā“š£®
½ā“š ½ā£ŗŌµē³ŲµÄ¹¹³ÉĢõ¼žŹĒ£ŗ1”¢ÓŠĮ½øö»īĘĆŠŌ²»Ķ¬µÄµē¼«£¬2”¢½«µē¼«²åČėµē½āÖŹČÜŅŗÖŠ£¬3”¢Į½µē¼«¼ä¹¹³É±ÕŗĻ»ŲĀ·£¬4”¢ÄÜ×Ō·¢µÄ½ųŠŠŃõ»Æ»¹Ō·“Ó¦£¬Ōµē³ŲÖŠÕż¼«ÉĻ·¢Éś»¹Ō·“Ó¦£¬øŗ¼«ÉĻ·¢ÉśŃõ»Æ·“Ó¦£¬¾Ż“ĖæÉÖŖ£ŗ
A£®µē¼«ĻąĶ¬£¬²»Äܹ¹³ÉŌµē³Ų£»
B£®Ć»ÓŠŠĪ³É±ÕŗĻ»ŲĀ·£¬²»Äܹ¹³ÉŌµē³Ų£»
C£®×°ÖĆCÖŠ¾Ę¾«ŹĒ·Ēµē½āÖŹ£¬²»Äܹ¹³ÉŌµē³Ų£»
D£®·ūŗĻ¹¹³ÉŌµē³ŲµÄĢõ¼ž£¬ÓŠµēĮ÷²śÉś£¬Ģś×÷øŗ¼«£¬Ķ×÷Õż¼«£¬¹¹³ÉĮĖ±ÕŗĻ»ŲĀ·£¬ŌŚøŗ¼«ĢśŹ§Č„µē×Ó£¬ŌŚÕż¼«ĒāĄė×ӵƵ½µē×Ó£¬
¹ŹŃ”D£®
µćĘĄ ±¾Ģāæ¼²éĮĖŌµē³ŲŌĄķµÄ·ÖĪöÓ¦ÓĆ£¬øĆĢāŹĒøßæ¼ÖŠµÄ³£¼ūæ¼µć£¬ŹōÓŚ»ł“”ŠŌŹŌĢāµÄ漲飬ÄŃ¶Č²»“ó£¬Ć÷Č·Ōµē³ŲµÄ¹¤×÷ŌĄķ”¢¹¹³ÉĢõ¼žŹĒ“šĢāµÄ¹Ų¼ü£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ŅŅĻ© | B£® | ±ūČ² | C£® | ŅģĪģĶé | D£® | ¶Ō¶ž¼×±½ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
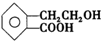 £¬ĖüæÉĶعż²»Ķ¬»Æѧ·“Ó¦·Ö±šÖʵĆB”¢C”¢DŗĶEĖÄÖÖĪļÖŹ£®
£¬ĖüæÉĶعż²»Ķ¬»Æѧ·“Ó¦·Ö±šÖʵĆB”¢C”¢DŗĶEĖÄÖÖĪļÖŹ£®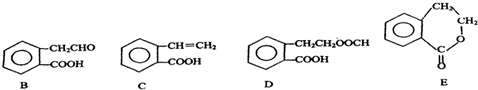
 £®
£® +2NaOH”ś
+2NaOH”ś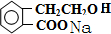 +HCOONa+H2O£®
+HCOONa+H2O£® £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | FeµÄĦ¶ūÖŹĮæĪŖ56g | |
| B£® | ³£ĪĀ³£Ń¹ĻĀ£¬71gCl2ŗ¬ÓŠNAøöCl2·Ö×Ó | |
| C£® | 1mol O2ŌŚ³£ĪĀĻĀµÄĢå»ż¶¼ĪŖ22.4L | |
| D£® | ½«1molNaCl¾§Ģå¼ÓČėµ½1LĖ®ÖŠ£¬µĆµ½NaClČÜŅŗµÄÅØ¶Č¾ĶŹĒ1mol•L-1 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 3 mol•L-1°±Ė® | B£® | 4 mol•L-1 HNO3 | ||
| C£® | 8 mol•L-1 NaOH | D£® | 18 mol•L-1 H2SO4 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 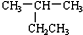 2-ŅŅ»ł±ūĶé 2-ŅŅ»ł±ūĶé | B£® | CH3CHØTCHCH3 ¶”Ļ© | ||
| C£® | 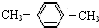 ¶Ō¶ž¼×±½ ¶Ō¶ž¼×±½ | D£® | 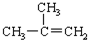 2-¼×»ł-2-±ūĻ© 2-¼×»ł-2-±ūĻ© |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¼×»łµÄµē×ÓŹ½£ŗ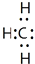 | B£® | 2-¶”Ļ©µÄ¼üĻߏ½£ŗ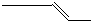 | ||
| C£® | ±ūĻ©µÄ½į¹¹¼ņŹ½£ŗCH2CHCH3 | D£® | ŅŅ“¼µÄ½į¹¹Ź½£ŗ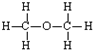 |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com