
| A. | KW均为1×10-14 | B. | 若a=12则b=2 | ||
| C. | a、b为固定值 | D. | 水电离出的c(H+)相等 |
分析 常温下pH=a的NaOH溶液与pH=b的硫酸溶液,将二者等体积混合,所得溶液为中性,说明氢离子与氢氧根离子恰好反应,
A.水的离子积只与温度有关;
B.氢离子与氢氧根离子的浓度相同;
C.10-a×10-b=1×10-14;
D.氢离子与氢氧根离子的浓度相同,对水的电离的抑制程度相同.
解答 解:常温下pH=a的NaOH溶液与pH=b的硫酸溶液,将二者等体积混合,所得溶液为中性,说明氢离子与氢氧根离子恰好反应,
A.水的离子积只与温度有关,常温下KW均为1×10-14,故A正确;
B.氢离子与氢氧根离子恰好反应,氢离子与氢氧根离子的浓度相同,所以若a=12,c(OH-)=10-2mol/L,则b=2,c(H+)=10-2mol/L,故B正确;
C.氢离子与氢氧根离子的浓度相同,则10-a×10-b=1×10-14,所以a+b=14,则a、b的值不固定,故C错误;
D.氢离子与氢氧根离子的浓度相同,对水的电离的抑制程度相同,所以水电离出的c(H+)相等,故D正确.
故选C.
点评 本题考查酸碱混合溶液定性判断,明确溶液中溶质及其性质是解本题关键,注意:酸或碱抑制水电离,氢离子与氢氧根离子浓度相同对水的电离抑制程度相同,题目难度不大.


 中考解读考点精练系列答案
中考解读考点精练系列答案科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
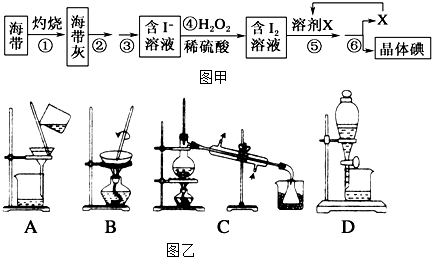
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

 ⑤
⑤ ⑥HOCH2CH2CH2COOH
⑥HOCH2CH2CH2COOH查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原CuSO4溶液的浓度为1mol/L | |
| B. | 若要使电解后的溶液恢复至电解前的CuSO4溶液,则需加入9.8gCu(OH)2固体 | |
| C. | 电解过程中转移电子数为0.4NA个 | |
| D. | 假设电解过程中忽略溶液体积变化,则电解后所得溶液中C(H+)=0.1mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
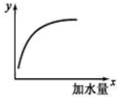 如图表示 25℃时,向 1L,0.1mol•L-1的一元弱酸HA中加水稀释过程的变化图象,则图中纵坐标y表示的是( )
如图表示 25℃时,向 1L,0.1mol•L-1的一元弱酸HA中加水稀释过程的变化图象,则图中纵坐标y表示的是( )| A. | c(H+)或 c(OH-) | B. | HA的电离平衡常数Ka | ||
| C. | c(H+)/c(HA) | D. | n(H+)或 n(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH3COOH(aq)+NaOH(aq)═CH3COONa(aq)+H2O(l)△H=-57.3kJ/mol | |
| B. | KOH(aq)+$\frac{1}{2}$H2SO4(aq)═$\frac{1}{2}$K2SO4(aq)+H2O(l)△H=-57.3kJ/mol | |
| C. | C8H18(l)+$\frac{25}{2}$ O2 (g)═8CO2 (g)+9H2O(g)△H=-5518 kJ/mol | |
| D. | 2C8H18(g)+25O2 (g)═16CO2 (g)+18H2O(1)△H=-5518 kJ/mol |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com