

| 元素代号 | A | B | D | E | G | H | J | L |
| 常见化合价 | -1 | -2 | +4、-4 | +6、+4、-2 | +5、-3 | +3 | +2 | +1 |
| 原子半径(pm) | 64 | 66 | 77 | 104 | 110 | 143 | 160 | 186 |
 (1)A、H、L对应离子的半径由大到小的顺序是(用离子符号表示) ;
(1)A、H、L对应离子的半径由大到小的顺序是(用离子符号表示) ; (2)A与L所形成的化合物的电子式 ;
(2)A与L所形成的化合物的电子式 ; (3)DB2的结构式为 ;
(3)DB2的结构式为 ; (4)D的最高正价氧化物与L的最高正价氧化物对应水化物X的溶液(足量)发生反应的离子方程式 ;
(4)D的最高正价氧化物与L的最高正价氧化物对应水化物X的溶液(足量)发生反应的离子方程式 ; (5)E的最高正价氧化物对应水化物y的浓溶液与Cu发生反应的化学方程式为
(5)E的最高正价氧化物对应水化物y的浓溶液与Cu发生反应的化学方程式为  。
。 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案科目:高中化学 来源:不详 题型:填空题
 (1)
(1) 与Ne原子电子层结构相同的
与Ne原子电子层结构相同的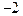 价阴离子,填写微粒的结构示意图: _____;
价阴离子,填写微粒的结构示意图: _____; (2)用电子式表示两核10电子的共价化合物形成过程: ;
(2)用电子式表示两核10电子的共价化合物形成过程: ; (3)在1~18号元素中,气态氢化物的水溶液呈碱性的化合物的结构式:__________ 。
(3)在1~18号元素中,气态氢化物的水溶液呈碱性的化合物的结构式:__________ 。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 P
P P
P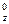 ,你认为同学甲所书写的电子排布式违背了下列选项中的
,你认为同学甲所书写的电子排布式违背了下列选项中的| A.能量最低原理 | B.泡利不相容原理 |
| C.洪特规则 | D.洪特的全充满、半充满、全空状态 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 、Y、Z在周期表中的位置如图所示,则下列说法正确的是 ( )
、Y、Z在周期表中的位置如图所示,则下列说法正确的是 ( )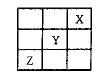
| A.Z一定是活泼的金属 |
| B.Y元素与第IA族的元素只能形成离子化合物 |
| C.X、Y、Z三种元素中X元素的得电子能力最强 |
| D.Z的最高价氧化物的水化物是强酸 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.酸性强弱:HBrO4>HClO4 | B.原子半径大小:Na>S |
| C.碱性强弱:NaOH>LiOH | D.还原性强弱:F-<Cl- |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.①④⑤ | B.②④⑥ | C.④⑤⑥ | D.③⑤⑥ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com