
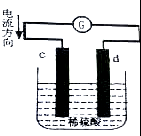
 如图是锌片和铜片同时插入稀硫酸中所组成的原电池装置,c,d为两个电极.则下列有关的判断不正确的是( )
如图是锌片和铜片同时插入稀硫酸中所组成的原电池装置,c,d为两个电极.则下列有关的判断不正确的是( )| A. | d为负极,电池工作时,d极发生氧化反应 | |
| B. | c为锌片,电池工作时,溶液中SO42-向c极移动 | |
| C. | 电池工作的过程中,d电极上产生大量的气泡 | |
| D. | 电池工作的过程中,溶液的pH基本不变 |
分析 根据图象知,c是负极、d是正极,Zn易失电子作负极、Cu作正极,所以c是Zn、d是Cu,负极反应式为Zn-2e-=Zn2+、正极反应式为2H++2e-=H2↑,放电时,电解质溶液中阳离子向正极移动,阴离子向负极移动,据此分析解答.
解答 解:据图象知,c是负极、d是正极,Zn易失电子作负极、Cu作正极,所以c是Zn、d是Cu,负极反应式为 Zn-2e-=Zn2+、正极反应式为2H++2e-=H2↑,
A.d是正极,正极上得电子发生还原反应,故A错误;
B.c为锌片,放电时,硫酸根离子向负极c移动,故B正确;
C.放电时,正极d上反应式为2H++2e-=H2↑,所以d电极上产生大量气泡,故C正确;
D.放电时,正极d上反应式为2H++2e-=H2↑,所以溶液中pH增大,故D错误;
故选AD.
点评 本题考查原电池原理,侧重考查学生对电流方向与电极正负极的关系是解本题关键,会正确书写电极反应式,题目难度不大.


 初中暑期衔接系列答案
初中暑期衔接系列答案科目:高中化学 来源: 题型:选择题
| A. | 制作餐具使用的不锈钢是合金 | B. | 富含淀粉的食物可用碘水来检验 | ||
| C. | 汽油和花生油均属于酯类 | D. | 蛋白质水解的最终产物是氨基酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 苯酚和羟基扁桃酸互为同系物 | |
| B. | 常温下,1mol羟基扁桃酸只能与1molBr2反应 | |
| C. | 此反应为加成反应,羟基扁桃酸分子中至少有12个原子共平面 | |
| D. | 乙醛酸的核磁共振氢谱中只有1个吸收峰 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 若A和C形成一种化合物CA,则CA属于离子化合物 | |
| B. | 原子半径的大小顺序:r(D)>r(C)>r(B)>r(A) | |
| C. | 由于化合物A2B形成氢键,所以热稳定性:A2B>A2D | |
| D. | 元素C的单质是一种高硬度、高熔点的金属 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 131是这种碘-131的质量数 | B. | $\underset{131}{53}$I与$\underset{127}{53}$I互为同位素 | ||
| C. | 碘-131的中子数为53 | D. | 碘元素在周期表中位于第ⅦA族 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向Ca(ClO)2中通入少量SO2:Ca2++2ClO-+SO2+H2O═CaSO3↓+2HClO | |
| B. | 醋酸与水垢中的CaCO3反应:CaCO3+2H+═Ca2++H2O+CO2↑ | |
| C. | 向AlCl3溶液中加入过量的氨水:Al3++4NH3•H2O═AlO2-+4NH4+ | |
| D. | NO2与水的反应:3NO2+H2O═2NO3-+NO+2H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 操作和现象 | 结论或目的 |
| A | 向红砖粉末中加入盐酸,充分反应后取上层清液于试管中,滴加KSCN溶液2~3滴,溶液呈红色 | 红砖中含有氧化铁 |
| B | CO还原Fe2O3得到的黑色固体加入盐酸溶解后再加入KSCN溶液,溶液不显红色 | 黑色固体中没有Fe3O4 |
| C | 取少量Fe(NO3)2试样加水溶解,加稀H2SO4酸化,滴加KSCN溶液,溶液变为红色 | 该Fe(NO3)2试样已经变质 |
| D | 向某溶液中通入Cl2,然后再加入KSCN溶液变红色 | 原溶液中含有Fe2+ |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
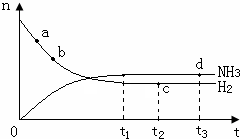 氨气是一种重要的化工原料,大量用于制造尿素、纯碱、铵态氮肥以及硝酸,在有机合成工业中制合成纤维、塑料、染料等.请回答下列问题:
氨气是一种重要的化工原料,大量用于制造尿素、纯碱、铵态氮肥以及硝酸,在有机合成工业中制合成纤维、塑料、染料等.请回答下列问题:| 容器编号 | 起始时各物质物质的量/mol | 平衡时反应 | ||
| N2 | H2 | NH3 | ||
| a | 1 | 3 | 0 | 23.1 |
| b | 2 | 6 | 0 | 未知(用E表示) |
| 容器 | c(CO2) /mol•L-1 | c(H2) /mol•L-1 | c(CH3OCH3) /mol•L-1 | c(H2O) /mol•L-1 | v (正)和v (逆)比较 |
| 容器I | 1.0×10-2 | 1.0×10-2 | 1.0×10-4 | 1.0×10-4 | v (正)=v (逆) |
| 容器II | 2.0×10-2 | 1.0×10-2 | 1.0×10-4 | 2.0×10-4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com