
分析 (1)①CO2(g)+3H2(g)?CH3OH(l)+H2O (g)△H=Q1kJ•mol-1
②CH3OH(l)+$\frac{1}{2}$O2(g)?CO2(g)+2H2(g)△H=Q2kJ•mol-1
③H2O(g)=H2O(l)△H=Q3kJ•mol-1,依据盖斯定律①×2+②×3+③×2得到所需热化学方程式;
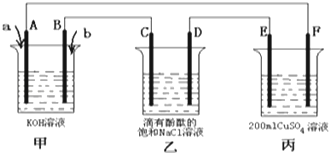
(2)甲为原电池,乙、丙为电解池,当向甲池通入气体a和b时,D极附近呈红色,说明D为电解池的阴极,C为电解池的阳极,b为正极,a为负极,E为阳极,F为阴极;
①a为甲醇电极商十点钟发生氧化反生成碳酸盐;
②乙中是电极饱和食盐水;
③依据电极反应和电子守恒计算所得溶液的PH.
解答 解:(1)①CO2(g)+3H2(g)?CH3OH(l)+H2O (g)△H=Q1kJ•mol-1
②CH3OH(l)+$\frac{1}{2}$O2(g)?CO2(g)+2H2(g)△H=Q2kJ•mol-1
③H2O(g)=H2O(l)△H=Q3kJ•mol-1,依据盖斯定律①×2+②×3+③×2得到:
表示甲醇的燃烧热的热化学方程式为CH3OH(l)+$\frac{3}{2}$O2(g)═CO2(g)+2H2O(l)△H=(2Q1+3Q2+2Q3) kJ•mol-1;
故答案为:CH3OH(l)+$\frac{3}{2}$O2(g)═CO2(g)+2H2O(l)△H=(2Q1+3Q2+2Q3) kJ•mol-1;
(2)甲为原电池,乙、丙为电解池,当向甲池通入气体a和b时,D极附近呈红色,说明D为电解池的阴极,C为电解池的阳极,b为正极,a为负极,E为阳极,F为阴极;
①上述分析可知a物质为甲醇,电极反应为:CH3OH-6e-+8OH-=CO32-+6H2O;
故答案为:CH3OH;CH3OH-6e-+8OH-=CO32-+6H2O;
②乙中是电极饱和食盐水,生成氯气和氢气、氢氧化钠溶液,反应的化学方程式为:2NaCl+2H2O $\frac{\underline{\;通电\;}}{\;}$2NaOH+Cl2↑+H2↑;
故答案为:2NaCl+2H2O $\frac{\underline{\;通电\;}}{\;}$2NaOH+Cl2↑+H2↑;
③当乙装置中C电极收集到224mL(标况下)气体时,生成氯气物质的量=$\frac{0.224L}{22.4L/mol}$=0.01mol,2Cl--2e-=Cl2↑,电子转移0.02mol,丙中电解硫酸铜的反应为:2CuSO4+2H2O$\frac{\underline{\;通电\;}}{\;}$2Cu+O2↑+2H2SO4,电子转移4mol,反应2mol硫酸铜,生成硫酸2mol,电子转移0.02mol,生成硫酸0.01mol,氢离子浓度=0.02mol,c(H+)=$\frac{0.02mol}{0.2L}$=0.1mol/L,溶液的pH=1
故答案为:1.
点评 本题考查了盖斯定律的计算应用,原电池原理的理解应用和电解池中溶液PH的计算应用,掌握基础是关键,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | ③ | B. | ① | C. | ④ | D. | ② |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
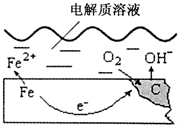 如图是钢铁在潮湿空气里发生电化学腐蚀的示意图,发生的反应为:2Fe+2H2O+O2═2Fe(OH)2.Fe(OH)2继续被氧化为Fe(OH)3,Fe(OH)3脱水生成铁锈.请根据图示,回答下列问题:
如图是钢铁在潮湿空气里发生电化学腐蚀的示意图,发生的反应为:2Fe+2H2O+O2═2Fe(OH)2.Fe(OH)2继续被氧化为Fe(OH)3,Fe(OH)3脱水生成铁锈.请根据图示,回答下列问题:| 物质 | 熔点/°C | 沸点/°C | 密度/g•cm-3 | 溶解性 |
| A | -11.5 | 198 | 1.11 | A、B互溶,且均易溶于水 |
| B | 17.9 | 290 | 1.26 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 相同温度下在水中的溶解度:Na2CO3<NaHCO3 | |
| B. | 相同浓度时pH大小关系为:Na2CO3<NaHCO3 | |
| C. | 等质量的两种固体,分别与过量盐酸反应,生成CO2的质量碳酸氢钠多 | |
| D. | 分别取1mol/L的两种溶液,滴入氯化钙溶液,两个皆有沉淀产生 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
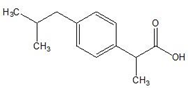 布洛芬缓释胶囊常用于缓解轻至中度疼痛如头痛、关节痛、偏头痛、牙痛、肌肉痛、神经痛、痛经.也用于普通感冒或流行性感冒引起的发热,布洛芬结构如图所示,下列关于布洛芬的说法正确的是( )
布洛芬缓释胶囊常用于缓解轻至中度疼痛如头痛、关节痛、偏头痛、牙痛、肌肉痛、神经痛、痛经.也用于普通感冒或流行性感冒引起的发热,布洛芬结构如图所示,下列关于布洛芬的说法正确的是( )| A. | 其分子式可以表示为C13H20O2 | |
| B. | 1mol该物质最多与4molH2加成 | |
| C. | 其核磁共振氢谱谱图有8个峰 | |
| D. | 该物质可发生氧化、还原、加成、消去、取代反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 纤维素与淀粉互为同分异构体 | |
| B. | 糖类、油脂、蛋白质都是高分子化合物,一定条件下均能水解 | |
| C. | 天然植物油常温下一般呈液态,难溶于水,有恒定的熔点、沸点 | |
| D. | 葡萄糖和蔗糖都含有C、H、O三种元素,但不是同系物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 蒸馏、分液、萃取 | B. | 萃取、蒸馏、分液 | C. | 分液、蒸馏、萃取 | D. | 蒸馏、萃取、分液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na 与水反应时,增大水的用量 | |
| B. | Fe 与稀硫酸反应制取氢气时,改用浓硫酸 | |
| C. | 在K2SO4与BaCl2两溶液反应时,增大压强 | |
| D. | 做铝与氧气反应的实验时,将铝片改为铝粉 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Al3+、K+、NO3-、Cl- | B. | K+、Na+、HS-、Cl- | ||
| C. | Na+、AlO2-、SO42-、NO3- | D. | Ba2+、Na+、Cl-、NO3- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com