
| A、1 | B、3 | C、4 | D、6 |
科目:高中化学 来源: 题型:
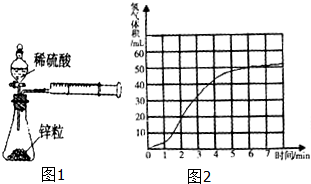 某课题组研究锌与稀硫酸的反应速率及影响因素,实验装置如图1所示.
某课题组研究锌与稀硫酸的反应速率及影响因素,实验装置如图1所示.| 编号 | 反应速率表达式的定义 | 反应速率表达式 | 反应速率单位 | ||
| ① | 单位时间内Zn2+物质的量浓度的增加量 | v(Zn2+)=
| mol/(L?min) | ||
| ② |
| 编号 | 锌的形状 | 锌的规格 | 硫酸的浓度 | 反应温度 | 实验设计的目的 |
| ① | 块状 | 纯锌 | 1mol/L | 25℃ | Ⅰ.实验①和②研究 Ⅱ.实验②和③研究 Ⅲ.实验③和④研究 Ⅳ.实验④和⑤研究 |
| ② | 颗粒状 | 纯锌 | 1mol/L | 25℃ | |
| ③ | 颗粒状 | 纯锌 | 25℃ | ||
| ④ | 颗粒状 | 2mol/L | 25℃ | ||
| ⑤ | 颗粒状 | 粗锌 | 2mol/L | 35℃ | |
| … | |||||
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
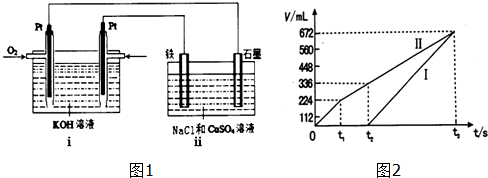
| 化合物 | 甲 | 乙 | 丙 | 丁 |
| 组成元素 | B、C | A、C | A、D | C、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、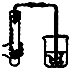 双手移去后,导管中水面与烧杯水面相平,则说明装置不漏气 |
B、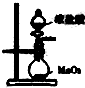 用于实验室制取Cl2 |
C、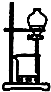 从海带中提取碘的实验过程中,用如图装置向烧杯中放出碘的苯溶液 |
D、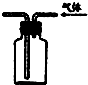 可用于实验室收集甲烷气体 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com