
| A. | 钢是用量最大的合金 | |
| B. | 铝锂合金抗腐蚀能力很强,可耐酸碱腐蚀 | |
| C. | 我国在商代就开始使用铜合金 | |
| D. | 铝合金的强度、硬度比纯铝大 |
科目:高中化学 来源: 题型:选择题
| A. | Mg、Ag | B. | Fe、Mg | C. | Al、Zn | D. | Mg、Al |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 反应时间/min | n(MgSO4)/mol | n(CO)/mol | n(SO2)/mol |
| 0 | 2.0 | 2.0 | 0 |
| 2 | 0.8 | ||
| 4 | 1.2 | ||
| 6 | 1.2 | 2.8 |
| A. | 0~2 min内的平均速率为υ(CO)=0.6 mol/(L•min) | |
| B. | 4 min后,平衡移动的原因可能是向容器中加入了2.0mol的SO2 | |
| C. | 4 min后,若升高温度,SO2物质的量浓度变为0.7mol/L,则正反应为放热反应 | |
| D. | 其他条件不变,若起始时容器中MgSO4、CO均为1.0mol,则平衡时n(SO2)=0.6mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | HSO3-+H20?SO32-+H3O+ | B. | S2-+H2O?H2S+2OH- | ||
| C. | Cu2++4H2O?Cu(OH)2+2H3O+ | D. | NH3•H2O+H3O+?NH4++2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH3-CH2-OH | B. | CH3-CH2-CH2-OH | ||
| C. | HO-CH2-CH2-CH2-OH | D. |  |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 可能呈酸性 | B. | 可能呈中性 | C. | 一定呈碱性 | D. | 一定呈中性 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
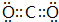 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 11:1 | B. | 9:2 | C. | 1:11 | D. | 2:9 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com