
分析 (1)根据元素化合价变化知,Pb失电子发生氧化反应作负极、PbO2得电子发生还原反应作正极;
(2)正极上PbO2得电子和硫酸根离子、氢离子反应生成硫酸铅和水;
(3)根据电池反应式知,放电过程中硫酸参加反应,所以随着反应的进行,氢离子浓度减小.
解答 解:(1)电池反应中Pb元素化合价由0价、+4价变为+2价,根据元素化合价变化知,氧化剂是PbO2,Pb失电子发生氧化反应作负极,故答案为:PbO2;Pb;
(2)正极上PbO2得电子和硫酸根离子、氢离子反应生成硫酸铅和水,正极反应式为PbO2+SO42-+2e-+4H+═PbSO4+2H2O,故答案为:PbO2+SO42-+2e-+4H+═PbSO4+2H2O;
(3)根据电池反应式知,放电过程中硫酸参加反应,所以随着反应的进行,氢离子浓度减小,所以溶液的pH变大,故答案为:变大;在过程中消耗了H2SO4.
点评 本题考查电极反应式的书写,侧重考查基本理论,明确元素化合价变化与正负极的关系是解本题关键,难点是电极反应式的书写,要结合电解质溶液酸碱性书写.


科目:高中化学 来源: 题型:选择题
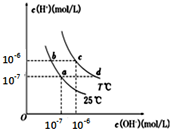
| A. | a点对应的溶液中大量存在:Na+、Mg2+、Cl-、SO42- | |
| B. | b点对应的溶液中大量存在:Fe2+、Ba2+、Cl-、NO3- | |
| C. | c点对应的溶液中大量存在:K+、Al3+、Cl-、CO32- | |
| D. | d点对应的溶液中大量存在:Na+、NH4+、ClO-、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | +135 KJ•mol-1 | B. | -375 KJ•mol-1 | C. | -325 KJ•mol-1 | D. | +325 KJ•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向水中加入稀氨水,水的电离平衡逆向移动,c(OH-)减小 | |
| B. | 向水中加入少量固体硫酸氢钠,c(H+)增大,KW不变 | |
| C. | 向水中加入少量固体CH3COO Na,水的电离平衡逆向移动,c(H+)减小 | |
| D. | 将水加热,KW增大,pH不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙醇与乙酸的反应 | |
| B. | 蛋白质的水解反应 | |
| C. | 苯和浓硝酸、浓硫酸混合液在50-60℃水浴中发生的反应 | |
| D. | 乙烯使溴水褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
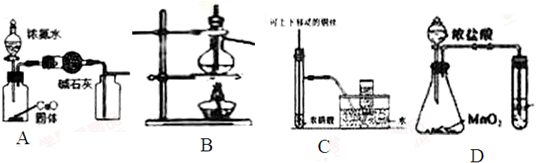
| A. | 制取并收集干燥纯净的NH3 | B. | 分离Br2和CCl4的混合物 | ||
| C. | 用于制备并收集少量NO | D. | 比较MnO2、Cl2、S 的氧化性 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | S(g)+O2(g)=SO2(g)放热为Q′,则Q′>Q | |
| B. | S(g)+O2(g)=SO2(g)放热为Q′,则Q′<Q | |
| C. | 1mol SO2(g)的能量>1mol S(s)的能量+1mol O2(g)的能量 | |
| D. | 1mol SO2(g)的能量<1mol S(s)的能量+1mol O2(g)的能量 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ | ⑩ |
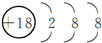 .
.| 实验步骤 | 实验现象与结论 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com