
��4�֣�NO��������Ⱦ����������������������������������NO����������������֯�д��ڣ���������Ѫ�ܣ���ǿ���ߺͼ���Ĺ��ܣ�����Ϊ��ǰ������ѧ���о��ȵ㣬NO�౻��Ϊ�����Ƿ��ӡ�����ش��������⡣
��1��NO�Ի�����Σ������
A���ƻ������� B����������ʹһЩ��������
C��������� D��������Ѫ�쵰���
��2���ں�Cu+ ���ӵ�ø�Ļ�����У�����������ӿ�ת��ΪNO��д��Cu+ �������������������ˮ��Һ�з�Ӧ�����ӷ���ʽ��___________________
��1��ACD ��2�� Cu+ + NO2��+ 2H+ 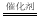 Cu2+ + NO��+ H2O
Cu2+ + NO��+ H2O
��������
�����������1��NO���������Ӧ���ƻ������㣬��NO����������ϣ���������������������γ�����ijɷ֣�����NO���γ����꣬CO��������Ѫ�쵰��������ж�����CO�ڸ�������ʹһЩ�������������ڶԻ����ĵ�Σ��������A��C��D��ȷ��ѡACD��
��2���ں�Cu+ ���ӵ�ø�Ļ�����У�����������ӿ�ת��ΪNO��˵����Ԫ�ػ��ϼ۽��ͣ��õ��ӣ���ͭԪ��ʧ���ӻ��ϼ����ߣ�����Cu+ �������������������ˮ��Һ�з�Ӧ�����ӷ���ʽΪCu+ + NO2��+ 2H+ 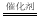 Cu2+ + NO��+ H2O��
Cu2+ + NO��+ H2O��
���㣺���鵪������������ʼ���Ի�����Ӱ�졣


 �ʰ�Ӣ��ͬ����ϰ��ϵ�д�
�ʰ�Ӣ��ͬ����ϰ��ϵ�д� ѧϰʵ����ϵ�д�
ѧϰʵ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�����ʡ��ˮ�и�������μ�⿼�����ۻ�ѧ�Ծ��������棩 ���ͣ������
(14��)����������Ԫ��A��B��C��D��Eԭ��������������A��Ԫ�����ڱ���ԭ�Ӱ뾶��С��Ԫ�أ�B���γɻ�������������Ԫ�أ�Cԭ�ӵ������������Ǵ�����������3����D��ͬ�����н�������ǿ��Ԫ�أ�E�ĸ�һ��������C��ij���⻯����Ӻ�����ͬ�ĵ�������
��1��A��C��D�γɵĻ������к��еĻ�ѧ������Ϊ ��
��2����֪��
�� E��E��2E ��H����a kJ/mol��
�� 2A��A��A ��H����b kJ/mol��
�� E��A��A��E ��H����c kJ/mol��
д��298Kʱ��A2��E2��Ӧ���Ȼ�ѧ����ʽ ��
��3����ij�¶����ݻ���Ϊ2L�������ܱ������У�����ͬ��ʽͶ�뷴Ӧ����ֺ��º��ݣ�ʹ֮������Ӧ��2A2(g)��BC(g) X(g) ��H����Q kJ/mol��Q��0��XΪA��B��C����Ԫ����ɵ�һ�ֻ��������ʼͶ����������ﵽƽ��ʱ���й��������£�
X(g) ��H����Q kJ/mol��Q��0��XΪA��B��C����Ԫ����ɵ�һ�ֻ��������ʼͶ����������ﵽƽ��ʱ���й��������£�
ʵ�� | �� | �� | �� |
��ʼͶ�� | 2 molA2��1 molBC | 1 molX | 4 molA2��2 molBC |
ƽ��ʱn(X) | 0.5mol | n2 | n3 |
��Ӧ�������仯 | �ų�Q1kJ | ����Q2kJ | �ų�Q3kJ |
��ϵ��ѹǿ | P1 | P2 | P3 |
��Ӧ���ת���� |
|
|
|
���ڸ��¶��£�����������ӷ�Ӧ��ʼ��ƽ������ʱ��Ϊ4 min����A2��ƽ����Ӧ����v (A2)= ��
�ڼ�����¶��´˷�Ӧ��ƽ�ⳣ��K = ��
�����������еķ�Ӧ�ֱ��ƽ��ʱ���и������ݹ�ϵ��ȷ���� ������ĸ����
A����1����2��1
B��Q1��Q2��Q
C����3����1
D��P3��2P1��2P2
E��n2��n3��1.0mol
F��Q3��2Q1
���������������������£��������������ѹ����1L�����ڵ�8min�ﵽ�µ�ƽ��ʱA2����ת����Ϊ75%��������ͼ�л�����5min ����ƽ��ʱX�����ʵ���Ũ�ȵı仯���ߡ�

��4������̼����ȼ�ϵ��(MCFC)��һ�ָ���ȼ�ϵ�أ�����Ϊ�ڶ���ȼ�ϵ�أ���δ�����÷��������ѡ��֮һ���乤��ԭ����ͼ��ʾ��

����A2(g)��BC(g)Ϊȼ�ϣ���һ������Li2CO3��Na2CO3���ۻ����Ϊ����ʡ�д����̼����ȼ�ϵ�أ�MCFC�������ĵ缫��Ӧʽ____________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�긣��ʡ������һ�����У������ѧ����ĩ��ѧ�Ծ��������棩 ���ͣ�ѡ����
�������и�װ��ͼ�������У���ȷ����
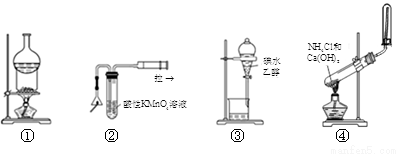
A��װ�âٿ����ڷ���I2��NH4Cl�����
B��װ�âڿ����ڼ�����ͷȼ�ղ�����SO2
C��װ�âۿ����Ҵ���ȡ��ˮ�еĵ�
D��װ�âܿ�����ʵ������ȡ���ռ���������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�갲��ʡ�����и�����һ��ģ�⿼�Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
��ѧƷ���ǽ�����װ�������ظ����ж�����ȼ���ӷ����и�ʴ�ԵĻ�ѧ���ʵĻ���������˵���������
A���ڴ����ĵײ�������Ƕͭ���Ա�������
B������ִ��տɴ�������ɢװ����������Һ
C���״���Ũ�������ֿ���������
D���촬���Ӹְ�ʱ���ö�����̼������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�갲��ʡ�����и�����һ��ģ�⿼�Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
�ڻ�ҩ��ըʱ�ɷ������·�Ӧ��5S��16KNO3��16C=3K2SO4��4K2CO3��K2S+12CO2����8N2���������й�˵����ȷ����
A����ԭ����ֻ��һ��
B��C����������Ҳ�ǻ�ԭ��
C���������뱻��ԭ��S���ʵ���֮��Ϊ3:1
D���ڻ�ҩ��ը�����жԻ����������Ⱦ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015�����ɽ�ظ߶���ѧ����ĩ���Ի�ѧ���ģ��Ծ��������棩 ���ͣ�ѡ����
������Դ���ķ����ǣ�
A������ B������ C���ѷʷ� D��������շ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015�����ɽ�ظ߶���ѧ����ĩ���Ի�ѧ���ģ��Ծ��������棩 ���ͣ�ѡ����
�������������������ǵ����ӡ��������������ڱ�����������
A����ֽ����ˮû������ֱ���ŷ� B���ƹ�ʹ��̫���ܵ��
C���綯�������沿��ȼ������ D������Դ���滯ʯ��Դ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015�����ɽ�ظ߶���ѧ����ĩ���Ի�ѧ�������Ծ��������棩 ���ͣ������
��12�֣���1��25��ʱ��pH=12.0��KOH��Һ�У���ˮ�������c��OH-��=_______mol/L��pH=12.0��K2CO3��Һ�У���ˮ���������c��OH-��=_______mol/L��
��2��������0.1mol��L-1 CH3COONa��ҺPH=8
�������ӷ���ʽ��ʾCH3COONa��ҺPH=8��ԭ��: ��
�ڰ����ʵ���Ũ���ɴ�С˳�����и���Һ�и�������ˮ���ӳ��⣩ ��
��3��FeCl3��ˮ��Һ�� ����ᡱ�����С���������ԣ�ԭ���ǣ������ӷ���ʽ��ʾ���� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015�㽭ʡ�����и�һ12���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
��ǿ���Ե���ɫ��Һ�У�һ�����Դ����������������
A��NH4����Na�� ��NO3�� ��Cl�� B��K�� ��Ba2�� ��Cl�� ��NO3��
C��K�� ��Na�� ��H����SO42�� D��Na����HS-��Cl����NO3��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com