
| A. | 42% | B. | 44% | C. | 48.6% | D. | 91.9% |
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
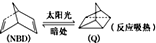 ,下列叙述中错误的是( )
,下列叙述中错误的是( )| A. | Q的能量高于NBD | B. | NBD和Q的分子式不同 | ||
| C. | Q的一氯代物只有3种 | D. | NBD的同分异构体可以是芳香烃 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分液、萃取、蒸馏 | B. | 萃取、分液、蒸馏 | C. | 萃取、蒸馏、分液 | D. | 分液、蒸馏、萃取 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
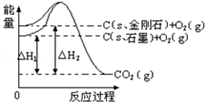
| A. | 金刚石的稳定性强于石墨 | |
| B. | 12g石墨总键能比12g金刚石小1.9kJ | |
| C. | 石墨和金刚石的转化是物理变化 | |
| D. | C(s、石墨)=C(s、金刚石)△H=+1.9 kJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.01 mol•L-1氨水溶液 | |
| B. | 0.02 mol•L-1氨水与0.02 mol•L-1HCl溶液等体积混合 | |
| C. | 0.03 mol•L-1氨水与0.01 mol•L-1 HCl溶液等体积混合 | |
| D. | pH=2的盐酸与pH=12的NaOH溶液等体积混合 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 开发太阳能、水能、风能、可燃冰等新能源、减少使用煤、石油等化石燃料 | |
| B. | 将煤进行气法处理,提高煤的综合利用效率 | |
| C. | 研究采煤、采油新技术,提高产量以满足工业生产的快速发展 | |
| D. | 实现资源的“3R”利用观,即:减 少资源消耗、增加资源的重复使用、奖励资源的循环再生使用 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA |
| 1 | ① | ||||||
| 2 | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |
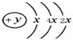 ,该位于周期表三周期IVA族;元素名称为硅,其最高价氧化物的化学式为SiO2.
,该位于周期表三周期IVA族;元素名称为硅,其最高价氧化物的化学式为SiO2.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com