
【题目】短周期元素W,X,Y,Z的原子序数依次增大,W与Y最外层电子数之和为X的最外层电子数的2倍,Z最外层电子数等于最内层电子数,X,Y,Z的简单离子的电子层结构相同,W的单质是空气中体积分数最大的气体。下列说法正确的是( )
A.Y的最高价氧化物对应水化物的酸性比W的强
B.W的气态氢化物比X的稳定
C.离子半径的大小顺序:r(W)>r(X)>r(Y)>r(Z)
D.XY2与ZY2中的化学键类型相同
【答案】C
【解析】短周期元素W、X、Y、Z 的原子序数依次增大,W的单质是空气中体积分数最大的气体,则W为N元素;Z最外层电子数等于最内层电子数,原子序数大于N元素,只能处于第三周期,故Z为Mg元素;X、Y、Z的简单离子的电子层结构相同,结构原子序数可知,X只能处于第二周期,且最外层电子数大于5,W(氮元素)与Y最外层电子数之和为X的最外层电子数的2倍,则Y原子最外层电子数只能为奇数,结合原子序数可知,Y不可能处于ⅠA族,只能处于ⅦA族,故Y为F元素,X最外层电子数为 ![]() =6,则X为O元素。W为N元素,最高价氧化物对应水化物为HNO3 , Y为F元素,没有最高正化合价,A项错误;非金属性O>N,故氢化物稳定性H2O>NH3 , B项错误;具有相同电子层结构的离子,核电荷数越大,离子半径越小,故离子半径r(N3-)>r(O2-)>r(F-)>r(Mg2+),C项正确;OF2中只含有共价键,MgF2中只含有离子键,二者化学键类型不同,D项错误。
=6,则X为O元素。W为N元素,最高价氧化物对应水化物为HNO3 , Y为F元素,没有最高正化合价,A项错误;非金属性O>N,故氢化物稳定性H2O>NH3 , B项错误;具有相同电子层结构的离子,核电荷数越大,离子半径越小,故离子半径r(N3-)>r(O2-)>r(F-)>r(Mg2+),C项正确;OF2中只含有共价键,MgF2中只含有离子键,二者化学键类型不同,D项错误。


 宝贝计划期末冲刺夺100分系列答案
宝贝计划期末冲刺夺100分系列答案 能考试全能100分系列答案
能考试全能100分系列答案科目:高中化学 来源: 题型:
【题目】短周期元素X,Y,Z,W在元素周期表中的相对位置如图所示,其中W原子的质子数是其最外层电子数的三倍,下列说法不正确的是( ) 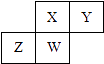
A.原子半径:W>Z>Y>X
B.最高价氧化物对应水化物的酸性:X>W>Z
C.最简单气态氢化物的热稳定性:Y>X>W>Z
D.元素X,Z,W的最高化合价分别与其主族序数相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式的书写正确的是( )
A.实验室用大理石和稀盐酸制取CO2:2H++CO ![]() =CO2↑+H2O
=CO2↑+H2O
B.铁和稀硝酸反应:Fe+2H+=H2↑+Fe2+
C.向AlCl3溶液中加入过量的NaOH溶液:Al3++3OH﹣=Al(OH)3↓
D.NaHCO3溶液与NaOH溶液反应:OH﹣+HCO ![]() =CO
=CO ![]() +H2O
+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铬是用途广泛的金属元素,但在生产过程中易产生有害的含铬工业废水.
(1)还原沉淀法是处理含Cr2O72﹣和CrO42﹣工业废水的一种常用方法,其工艺流程为:CrO42﹣ ![]() Cr2O72﹣
Cr2O72﹣ ![]() Cr3+
Cr3+ ![]() Cr(OH)3↓
Cr(OH)3↓
其中第Ⅰ步存在平衡:
2CrO42﹣(黄色)+2H+Cr2O72﹣(橙色)+H2O
①若平衡体系的pH=0,该溶液显色.
②根据2CrO42﹣+2H+Cr2O72﹣+H2O,设计如右图装置(均为惰性电极)电解Na2CrO4溶液制取Na2Cr2O7 . Na2Cr2O7中铬元素的化合价为 , 图中右侧电极连接电源的极,其电极反应式为 .
③第Ⅱ步反应的离子方程式: .
(2)CrO3具有强氧化性,遇到有机物(如酒精)时,猛烈反应以至着火.若该过程中乙醇被氧化成乙酸,CrO3被还原成绿色的Cr2(SO4)3 . 完成该反应的化学方程式:
□CrO3+□C2H5OH+□H2SO4═□Cr2(SO4)3+□CH3COOH+□
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图中A,B,C分别是三种有机物分子的表示方法: 
请回答下列问题:
①A,B两种模型分别是有机物的模型和模型.
②A,B,C三种有机物中,所有原子均共面的是(填字母序号).
③有机物C具有的结构或性质是(填字母序号).
a.是碳碳双键和碳碳单键交替的结构
b.有特殊气味、有毒、易溶于水、密度比水大
c.一定条件下能与液溴发生取代反应
d.能与浓硝酸发生氧化反应.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有A、B、C、D四块金属片,用导线两两相连插入稀硫酸中,可以组成各种原电池。若A和B相连时,A为负极;C与D相连时,C溶解,D上有氢气生成;A与C相连时,C为正极;B与D相连时,电子由D极经导线流向B极,则这四种金属的活泼性由强到弱的顺序为( )
A. ABCDB. ACDBC. CADBD. BDCA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酰氯(SO2Cl2)常作氯化剂或氯磺化剂,用于制作药品、染料、表面活性剂等。有关物质的部分性质如下表:
物质 | 熔点/℃ | 沸点/℃ | 其它性质 |
SO2Cl2 | -54.1 | 69.1 | ①易水解,产生大量白雾 |
H2SO4 | 10.4 | 338 | 吸水性且不易分解 |
实验室用干燥、纯净的二氧化硫和氯气合成硫酰氯,装置如图所示(夹持仪器已省略),请回答有关问题:
(1)仪器A冷却水的进水口为(填“a”或“b”)。
(2)仪器B中盛放的药品是。
(3)实验时,装置丁中发生反应的离子方程式为。
(4)装置丙的作用为 , 若缺少装置乙,则硫酰氯会水解,该反应的化学
方程式为。
(5)少量硫酰氯也可用氯磺酸(ClSO3H)分解获得,该反应的化学方程式为:2ClSO3H=H2SO4+ SO2Cl2 , 此方法得到的产品中会混有硫酸。
①从分解产物中分离出硫酰氯的方法是。
②请设计实验方案检验产品中有硫酸(可选试剂:稀盐酸、稀硝酸、BaCl2溶液、蒸馏水、石蕊溶液):。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com