
经氯气消毒的自来水,若用于配置以下溶液:①NaOH ②AgNO3 ③Na2CO3 ④FeSO4 ⑤KI ⑥NaCl ⑦Na2SO3不会使配置的溶液变质的是 ( )
A.全部 B.②④⑤⑥ C.②⑤ D.⑥
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源:2017届江西省赣州市十四校高三上期中联考化学试卷(解析版) 题型:选择题
2016年8月5日在巴西里约召开的第31届奥运会,由于兴奋剂事件而使多名俄罗斯运动员遭到禁赛,禁止运动员使用兴奋剂是奥运会公平、公正的重要举措之一。以下有两种兴奋剂的结构分别为:
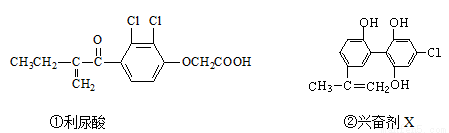
则关于以上两种兴奋剂的说法中正确的是 ( )
A.1mol利尿酸分子最多能和6molH2发生加成反应。
B.1mol兴奋剂X与足量浓溴水反应,最多消耗3molBr2
C.利尿酸分子中有三种含氧官能团,在核磁共振氢谱上共有六个峰
D.两种兴奋剂最多都能和含5molNaOH的溶液反应
查看答案和解析>>
科目:高中化学 来源:2017届广东省高三10月月考化学卷(解析版) 题型:选择题
下列装置、操作能达到目的或实验现象正确的是( )
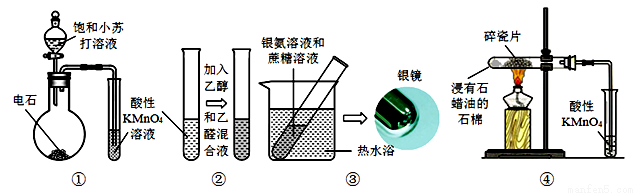
A.装置①:制取乙炔并验证炔烃的性质
B.装置②:检验乙醛的还原性,溶液颜色从紫红色变无色
C.装置③:产生银镜,说明蔗糖分子中含有醛基官能团
D.装置④:酸性KMnO4溶液中出现气泡且逐渐褪色,说明有不同于烷烃的另一类烃产生
查看答案和解析>>
科目:高中化学 来源:2017届天津市高三上质量调查二化学卷(解析版) 题型:选择题
下列说法中正确的是( )
A.分离Al2O3与Fe2O3混合物可以采取加入过量NaOH溶液充分反应后,过滤、洗涤、干燥
B.用过量氨水除去Fe3+溶液中的少量Al3+
C.将Fe(OH)3放入表面皿中,加入足量盐酸,将反应后的溶液加热蒸干、灼烧得到Fe2O3
D.Al(OH)3中混有Mg(OH)2加入足量烧碱溶液,充分反应过滤,向滤液中加入足量盐酸后过滤、洗涤、干燥
查看答案和解析>>
科目:高中化学 来源:2017届天津市高三上质量调查二化学卷(解析版) 题型:选择题
将磁性氧化铁放入稀HNO3中发生如下反应:3Fe3O4+28HNO3=9Fe(NO3)x+NO↑+14H2O下列判断合理的是( )
A.中Fe(NO3)x的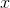 为2
为2
B.反应中每生成0.1mol还原产物,就有0.6mol电子转移
C.稀HNO3在反应中只作氧化剂
D.磁性氧化铁中的铁元素部分被氧化
查看答案和解析>>
科目:高中化学 来源:2017届天津市高三上质量调查二化学卷(解析版) 题型:选择题
下列说法不正确的是( )
A.当7.8 g Na2O2与H2O完全反应时,有0.1 mol电子发生了转移
B.FeCl2溶液与NaOH溶液混合,利用此反应可检验Fe2+
C.用浓盐酸酸化KMnO4溶液以增强其氧化性
D.在3NO2+H2O=2HNO3+NO中,氧化剂和还原剂的质量 比为1:2
比为1:2
查看答案和解析>>
科目:高中化学 来源:2017届四川省资阳市高三上第一次诊断化学试卷(解析版) 题型:推断题
【化学—选修5:有机化学基础】
已知化合物I的分子式为C11H14O2,其合成路线如图所示:
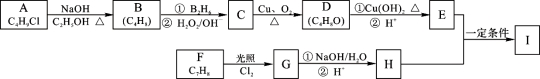
查阅资料有如下信息:i A的核磁共振氢谱表明其只有一种化学环境的氢;
ii 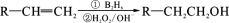 ;
;
iii F为苯的同系物。
请回答下列问题:
(1)A的结构简式为_____________,D所含官能团的名称是_____________。
(2)C的名称为_____________,H的分子式为_____________。
(3)A→B、F→G的反应类型分别为_____________、_____________。
(4)写出C→D反应的化学方程式:_____________。
(5)I的结构简式为_____________。
(6)I的同系物J比I的相对分子质量小14,J的同分异构体中能同时满足如下条件:①苯环上只有两个取代基,②能与饱和NaHCO3溶液反应放出CO2,共有_________种(不考虑立体异构)。其中核磁共振氢谱为五组峰,且峰面积比为1∶2∶2∶1∶6,写出J的这种同分异构体的结构简式_________。
查看答案和解析>>
科目:高中化学 来源:2017届四川省泸州市高三上10月月考化学卷(解析版) 题型:选择题
某无色溶液中可能含有①Na+、②Ba2+、③Cl-、④Br-、⑤SO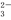 、⑥SO
、⑥SO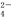 中的若干种,依次进行下列实验,且每步所加试剂均过量,观察到的现象如下:
中的若干种,依次进行下列实验,且每步所加试剂均过量,观察到的现象如下:
步骤 | 操作 | 现象 |
(1) | 用pH试纸检验 | 溶液的pH大于7 |
(2) | 向溶液中滴加氯水,再加入CCl4振荡,静置 | CCl4层呈橙色 |
(3) | 向(2)所得的水溶液中加入Ba(NO3)2溶液和稀硝酸 | 有白色沉淀产生 |
(4) | 过滤,向滤液中加入AgNO3溶液和稀硝酸 | 有白色沉淀产生 |
下列结论正确的是( )
A. 不能确定的离子是① B. 不能确定的离子是③⑤
C. 肯定含有的离子是①④⑤ D. 肯定没有的离子是②⑤
查看答案和解析>>
科目:高中化学 来源:2017届山东省栖霞市高三上学期期中化学试卷(解析版) 题型:实验题
化学小组设计以下实验方案,测定某部分变质为碳酸钠的小苏打样品中NaHCO3的质量分数。
(1)方案一:称取一定质量样品,置于仪器a中用酒精灯加热至恒重,冷却,用托盘天平称量剩余固体质量。重复操作,计算。
仪器a的名称是____________;其中发生反应的化学方程式为_______________。实验中为保证NaHCO3分解完全需加热至恒重,判断方法是________________。
⑵方案二:称取一定质量样品,置于小烧杯中,加适量水溶解;向小烧杯中加入足量Ba(OH)2溶液,待沉淀后,过滤,洗涤,干燥,称量固体质量,计算。
写出NaHCO3与足量Ba(OH)2溶液反应的离子方程式_______________;实验中判断沉淀是否完全的方法是______________。过滤操作中,除烧杯、漏斗外,还要用到的玻璃仪器为____________。
(3)方案三:称取一定质量样品,按如图装置进行实验:
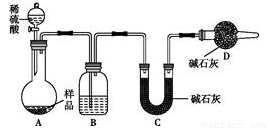
B装置内所盛试剂是;D装置的作用是______________。实验前称取17.9g样品,实验后测得C装置增重8.8g,则样品中NaHCO3的质量分数为________。某同学认为上述测定结果__________(填“偏高”或“偏低”),因为实验装置还存在一个明显的缺陷是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com