
用化学用语填空
(1)判断以下常见分子的中心原子的杂化轨道类型(用序号填空).
①+ ②CH2O ③NH3 ④SO2 ⑤BeCl2 ⑥H2O ⑦CO2
sp3杂化的是 ,sp2杂化的是 ,sp杂化的是 .
(2)下列物质中,只含有极性键的分子是 ,既含离子键又含共价键的化合物是 ;只存在σ键的分子是 ,同时存在σ键和π键的分子是 .
A.N2 B.CO2 C.CH2Cl2 D.C2H4 E.C2H6 F.CaCl2 G.NH4Cl.
考点:
原子轨道杂化方式及杂化类型判断;化学键.
分析:
(1)根据价层电子对互斥理论确定原子杂化方式,价层电子对个数=σ键个数+孤电子对个数,σ键个数=配原子个数,孤电子对个数=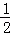 ×(a﹣xb),a指中心原子价电子个数,x指配原子个数,b指配原子形成稳定结构需要的电子个数,据此判断杂质类型;
×(a﹣xb),a指中心原子价电子个数,x指配原子个数,b指配原子形成稳定结构需要的电子个数,据此判断杂质类型;
(2)非金属元素的原子之间通常形成共价键,不同种非金属元素原子之间通常形成极性键,同种非金属元素原子之间形成非极性键,活泼金属和活泼非金属元素之间易形成离子键;
只含共价键的化合物是共价化合物,离子键为阴阳离子之间形成的化学键,离子化合物中一定含有离子键,可能含有共价键;
只存在共价单键的分子中只含σ键,含有双键、三键的分子中存在σ键和π键.
解答:
解:(1)①NH4+中N原子杂化轨道数为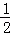 ×(5+4﹣1)=4,采取sp3杂化方式;
×(5+4﹣1)=4,采取sp3杂化方式;
②HCHO中碳原子成2个C﹣Hσ键,1个碳氧双键,双键中含有1个σ键、1个π键,杂化轨道数为2+1=3,所以碳原子采取sp2杂化;
③NH3中价层电子对个数=σ键个数+孤电子对个数=3+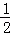 ×(5﹣3×1)=4,中心原子是以sp3杂化;
×(5﹣3×1)=4,中心原子是以sp3杂化;
④SO2中S原子形成2个σ键,孤电子对个数=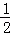 ×(6﹣2×2)=1,价层电子对数为3,为sp2杂化;
×(6﹣2×2)=1,价层电子对数为3,为sp2杂化;
⑤BeCl2中价层电子对个数=σ键个数+孤电子对个数=2+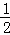 ×(2﹣2×1)=2,中心原子是以sp杂化;
×(2﹣2×1)=2,中心原子是以sp杂化;
⑥H2O中O原子的价层电子对个数=2+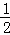 (6﹣2×1)=4,所以O原子采用sp3杂化;
(6﹣2×1)=4,所以O原子采用sp3杂化;
⑦二氧化碳分子中价层电子对个数=σ键个数+孤电子对个数=2+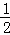 (4﹣2×2)=2,采取sp杂化方式;
(4﹣2×2)=2,采取sp杂化方式;
故答案为:①③⑥;②④;⑤⑦;
(2)A.N2分子含有非极性共价键,属于单质,氮气分子结构简式为N≡N,所以氮气分子中含有σ键和π键;
B.CO2分子中碳原子和氧原子之间存在极性键,属于共价化合物,二氧化碳分子结构简式为O=C=O,所以二氧化碳分子中含有σ键和π键;
C.CH2Cl2分子中碳原子和氢原子或氯原子之间存在极性键,属于共价化合物,CH2Cl2分子结构式为: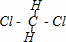 ,CH2Cl2分子中只含σ键;
,CH2Cl2分子中只含σ键;
D.C2H4分子中碳原子和氢原子之间存在极性键,碳原子和碳原子之间存在非极性共价键,属于共价化合物,乙烯的结构式为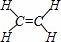 ,乙烯分子中含有σ键和π键;
,乙烯分子中含有σ键和π键;
E.C2H6分子中碳原子和氢原子之间存在极性键,碳原子和碳原子之间存在非极性共价键,属于共价化合物,乙烷的结构式为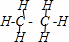 ,乙烷分子中只含σ键;
,乙烷分子中只含σ键;
F.CaCl2中只含离子键,属于离子化合物;
G.NH4Cl中铵根离子和氯离子之间存在离子键,氮原子和氢原子之间存在共价键,属于离子化合物,铵根离子中氮原子和氢原子之间存在σ键;
故答案为:BC;G;CE;ABD.
点评:
本题考查了原子杂化类型的判断、化学键类型的判断,题目难度中等,原子杂化类型的判断是高考的热点,根据“杂化轨道数=σ键数+孤对电子对数”解答,注意离子键与共价键的区别,注意极性共价键和非极性共价键的区别.


科目:高中化学 来源: 题型:
现有下列物质,用编号填空回答下列问题:
A.干冰 B.金刚石 C.氦 D.过氧化钠 E.二氧化硅 F.溴化铵
(1)通过非极性键形成的原子晶体是: .
(2)可由原子直接构成的晶体是: .
(3)含有离子键、共价键、配位键的化合物是: .
(4)含有非极性键的离子化合物是: .
(5)已知微粒间的作用力包括离子键、共价键、金属键、范德华力、氢键.氯化钠熔化,粒子间克服的作用力为 ;二氧化硅熔化,粒子间克服的作用力为 ;干冰气化,粒子间克服的作用力为 .A、B、C、D四种物质的熔点从低到高的顺序为 (填序号).
查看答案和解析>>
科目:高中化学 来源: 题型:
关于原子轨道的说法正确的是( )
|
| A. | 凡是中心原子采取sp3杂化方式成键的分子其几何构型都是正四面体 |
|
| B. | CH4分子中的sp3杂化轨道是由4个H原子的1s轨道和C原子的2p轨道混合起来而形成的 |
|
| C. | sp3杂化轨道是由同一个原子中能量相近的s轨道和p轨道混合起来形成的一组能量相同的新轨道 |
|
| D. | 凡AB3型的共价化合物,其中心原子A均采用sp3杂化方式成键 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列化学用语书写正确的是( )
|
| A. | 次氯酸的结构式:H﹣Cl﹣O |
|
| B. | 氯化镁的电子式: |
|
| C. | 作为相对原子质量测定标准的碳核素:614C |
|
| D. | 用电子式表示氯化氢分子的形成过程: |
查看答案和解析>>
科目:高中化学 来源: 题型:
为探究原电池的形成条件和反应原理,某同学设计了如下实验并记录了现象:①向一定浓度的稀硫酸中插入锌片,看到有气泡生成;②向上述稀硫酸中插入铜片,没有看到有气泡生成;③将锌片与铜片上端接触并捏住,一起插入稀硫酸中,看到铜片上有气泡生成,且生成气泡的速率比实验①中快;④在锌片和铜片中间接上电流计,再将锌片和铜片插入稀硫酸中,发现电流计指针偏转.下列关于以上实验设计及现象的分析,不正确的是( )
|
| A. | 实验①、②说明锌能与稀硫酸反应而铜不能 |
|
| B. | 实验③说明发生原电池反应时会加快化学反应速率 |
|
| C. | 实验③说明在该条件下铜可以与稀硫酸反应生成氢气 |
|
| D. | 实验④说明该原电池中铜为正极、锌为负极 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法中正确的是( )
|
| A. | 卤代烃在NaOH存在下水解生成的有机物都是醇 |
|
| B. | 所有的一元醇都能被氧化为具有相同碳原子数的醛或酮 |
|
| C. |
|
|
| D. | 分子式为C3H8与C6H14的两种有机物一定互为同系物 |
查看答案和解析>>
科目:高中化学 来源: 题型:
菜谱中记载:河虾不宜与西红柿同食。主要原因是河虾中含有五价砷,西红柿中含有比较多的维生素C,两者同食时会生成有毒的+3价砷。下列说法中正确的是 ( )
A.在该反应中维生素C作催化剂
B.砒霜是砷的氧化物,由上述信息可推知砒霜中含有的砷可能是+3价砷
C.因为河虾中含有砷元素,所以不能食用 D.上述反应中维生素C作氧化剂
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com