


分析 (1)A.依据m=CVM计算需要溶质的质量;
B.依据托盘天平使用方法结合氢氧化钠的腐蚀性解答;
C.依据量筒精确度解答;
D.依据配制溶液体积结合容量瓶规格选择;
E.将配制好一定物质的量浓度的溶液,注入刚用水洗净的试剂瓶中,相当把溶液稀释;
(2)依据容量瓶构造解答;
(3)依据配制一定物质的量浓度溶液一般步骤选择需要仪器;浓硫酸稀释时应将浓硫酸沿着烧杯壁缓缓注入水中,玻璃棒引流时,玻璃棒下端应靠在刻度线一下,仰视体积偏大;
(4)试剂瓶标签上应注明浓度和药品名称;
(5)根据c=$\frac{n}{V}$分析判断误差,如果n偏小或V偏大则配制溶液浓度偏低.
解答 解:(1)A.配制0.1mol/L CuSO4溶液100mL,需称量CuSO4•5H2O 0.1mol/L×0.1L×250g/mol=2.5g,故A错误;
B.托盘天平称量固体遵循左物右码,应将物品放置在左盘称量,氢氧化钠具有腐蚀性,应放在小烧杯中称量,故B错误;
C.量筒精确度为0.1mL,故C错误;
D.需要235mL 0.9mol/L NaCl溶液,实验室没有235mL容量瓶,应选择250mL容量瓶,故D正确;
E.将配制好一定物质的量浓度的溶液,注入刚用水洗净的试剂瓶中,相当把溶液稀释,溶液浓度偏低,故E错误;
故选:D;
(2)容量瓶为配制一定物质的量浓度溶液的专用仪器,容量瓶上标有:温度、容积、刻度线;
故选:BCE;
(3)配制一定物质的量浓度溶液一般步骤:计算、量取、稀释、冷却、移液、洗涤、定容、摇匀等,用到的仪器:量筒、胶头滴管、玻璃棒、烧杯、容量瓶,配制500mL溶液需要500mL容量瓶,所需的玻璃仪器除烧杯、量筒、玻璃棒和胶头滴管之外,还需要500mL容量瓶;
故答案为:500mL容量瓶;浓硫酸稀释时应将浓硫酸沿着烧杯壁缓缓注入水中,玻璃棒引流时,玻璃棒下端应靠在刻度线一下,仰视体积偏大,所以错误的操作为:1、2、4;
故答案为:1、2、4;
(4)试剂瓶标签上应注明浓度和药品名称: 或
或 ;
;
(5)A.容量瓶用蒸馏水洗净后,未等内壁干燥便用来配制,对溶液的体积,溶质的物质的量都不会影响,溶液浓度不变,故A不选;
B.烧碱在烧杯里刚好完全溶解,立即把溶液转移到容量瓶中,冷却后溶液体积偏小,溶液浓度偏大,故B不选;
C.定容时,仰视刻度线,导致溶液体积偏大,溶液浓度偏低,故C选;
D.摇匀静置后,发现液面未到刻度线,继续补加水至刻度线,导致溶液体积偏大,溶液浓度偏低,故D选;
E.在溶解过程中有少量液体溅出烧杯外,都在部分溶质损耗,溶质代物的量偏小,溶液浓度偏低,故E选;
故选:CDE.
点评 本题考查配制一定物质的量浓度的溶液,明确配制原理及操作是解题度不关键,注意根据$\frac{n}{V}$进行误差分析的方法,题目难度不大.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 8 L 0.2mol/L的Na2SO4溶液 | B. | 8 L0.15mol/L的Na3PO4溶液 | ||
| C. | 10 L0.1 mol/L的Na2CO3溶液 | D. | 2 L 0.5mol/L的NaCl溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
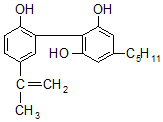
| A. | 该物质属于芳香烃 | |
| B. | 1mol该物质最多能与7molH2加成 | |
| C. | 该物质分子结构中存在7个碳碳双键 | |
| D. | 该物质能使酸性KMnO4溶液褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ①③ | C. | ②③ | D. | ②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题

| A. | 乙、丙都能发生银镜反应 | |
| B. | 用FeCl3溶液鉴别甲、丙两种有机化合物 | |
| C. | 甲分子中所有碳原子可能共平面 | |
| D. | 甲、乙、丙三种有机化合物均可与NaOH溶液发生反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ③①②④ | B. | ④③②① | C. | ①④②③ | D. | ②①④③ |
查看答案和解析>>
科目:高中化学 来源:2017届吉林省高三上第二次模拟化学试卷(解析版) 题型:选择题
如下流程示意图是用无机矿物资 源生产部分材料。
源生产部分材料。 下列有关说法不正确的是
下列有关说法不正确的是
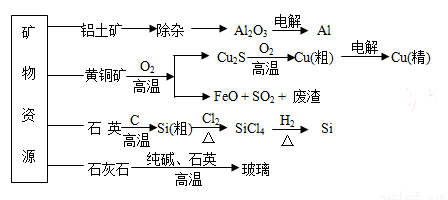
A.制取玻璃的同时产生CO2气体,制取粗硅时生成的气体产物为CO
B.生产高纯硅、铝、铜及玻璃的过程中都涉及氧化还原反应
C.粗硅制高纯硅时,提纯四氯化硅可用多次蒸馏的方法
D.黄铜矿冶炼铜时产生的SO2可用于生产硫酸 ,FeO可用作冶炼铁的原料
,FeO可用作冶炼铁的原料
查看答案和解析>>
科目:高中化学 来源:2017届广东省山一高三上第二次统测化学试卷(解析版) 题型:选择题
NA为阿伏加德罗常数的值。下列说法正确的是( )
A.18 g D2O和18 g H2O中含有的质子数均为10NA
B.14 g CO、C2H4混合气体与11.2 L N2所含有的分子数都是0.5NA
C.过氧化钠与水反应时,生成0.1 mol氧气转移的电子数为0.2NA
D.密闭容器中2 mol NO与1 mol O2充分反应,产物的分子数为2NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com