
| A. | ①③⑦ | B. | 只有⑦ | C. | ②④⑤⑦ | D. | ⑤⑥⑧ |
分析 ①原子晶体是原子之间通过共价键形成的晶体,同种原子之间形成的共价键是非极性键,不同元素形成的共价键是极性键,二氧化硅是原子晶体,晶体中存在极性键;
②稀有气体是单原子分子,可以形成分子晶体;
③二氧化硫常温下是气体,而硫是固体;
④Mg2+半径小于Ca2+半径,固MgO晶格能大于CaO晶格能,所以Mg2+比Ca2+更易与碳酸根离子中的氧离子结合,使碳酸根离子分解为CO2;
⑤分子晶体的堆积一般为分子密堆积,但有氢键时,配位数改变;
⑥离子晶体固态时不导电;
⑦离子晶体由阴、阳离子通过离子键形成,金属晶体是金属离子与自由电子通过金属键形成;
⑧依据构成微粒与微粒间的作用可将晶体分为金属晶体、离子晶体、分子晶体、原子晶体.
解答 解:①二氧化硅是原子晶体,晶体中存在极性键,故错误;
②稀有气体是单原子分子,可以形成分子晶体,故错误;
③二氧化硫常温下是气体,而硫是固体,所以SO2熔沸点低于S,故错误;
④Mg2+半径小于Ca2+半径,固MgO晶格能大于CaO晶格能,所以Mg2+比Ca2+更易与碳酸根离子中的氧离子结合,使碳酸根离子分解为CO2,所以碳酸钙比分解温度比碳酸镁的温度高,故错误;
⑤分子晶体的堆积一般为分子密堆积,但有氢键时,配位数改变,如由于氢键的作用,每个水分子周围只有四个紧邻的水分子,故错误;
⑥离子晶体固态时不导电,如氯化钠固体不导电,故错误;
⑦离子晶体由阴、阳离子通过离子键形成,金属晶体是金属离子与自由电子通过金属键形成,不存在离子键,故正确;
⑧依据构成微粒与微粒间的作用可将晶体分为金属晶体、离子晶体、分子晶体、原子晶体,故错误.
故选B.
点评 本题考查晶体类型与结构、化学键等,难度不大,注意稀有气体是单原子分子,不存在化学键,形成分子晶体.


 学而优衔接教材南京大学出版社系列答案
学而优衔接教材南京大学出版社系列答案科目:高中化学 来源: 题型:选择题
| A. | 12C与14C | B. | CH3CH2OH与CH3COOH | ||
| C. | 甲烷与丙烷 | D. | CH3CH2CH2CH3与CH3CH(CH3)2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 2 | ⑥ | ⑦ | ||||||
| 3 | ① | ③ | ⑤ | ⑧ | ⑩ | |||
| 4 | ② | ④ | ⑨ |
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 .它是由乙烯和对二甲苯经过一系列反应后的产物缩聚而成的,则合成过程中乙烯与对二甲苯的物质的量之比为( )
.它是由乙烯和对二甲苯经过一系列反应后的产物缩聚而成的,则合成过程中乙烯与对二甲苯的物质的量之比为( )| A. | 1:1 | B. | 2:1 | C. | 1:2 | D. | 3:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | CH2═CH2+HCl$\stackrel{一定条件}{→}$CH3CH2Cl | B. | CH4+Cl2$\stackrel{光照}{→}$CH3Cl+HCl | ||
| C. | C2H4+3O2$\stackrel{点燃}{→}$2CO2+2H2O | D. | 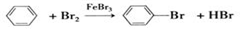 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ③⑤④⑤② | B. | ③⑤② | C. | ③⑤①② | D. | ③⑤①⑤② |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH4+Cl2$\stackrel{光}{→}$CH3Cl+HCl | |
| B. | 乙烯的燃烧:CH2=CH2+3O2$\stackrel{点燃}{→}$ 2CO2+2H2O | |
| C. | Fe2O3+6HCl═2FeCl3+3H2O | |
| D. | Na2CO3+H2O+CO2═2NaHCO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烯的结构简式为:CH2CH2 | B. | H2O的电子式: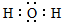 | ||
| C. | 葡萄糖的分子式:C12H22O11 | D. | 14C的原子结构示意图: |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com