
| A. | 2Q1>Q3>Q2 | B. | Q3>Q2>2Q1 | C. | Q2>Q3>2Q1 | D. | Q3>2Q1>Q2 |
分析 先根据温度变化,平衡移动判断反应a、反应b的热效应,然后利用盖斯定律判断.
解答 解:当温度降低时,反应a的平衡向正反应方向移动,说明该反应正向为放热反应,△H<0,反应b的平衡向逆反应方向移动,说明该反应正向为吸热反应,△H>0,
(1)C(s)+2H2(g)?CH4(g)△H=-Q1 kJ/mol
(2)2C(s)+H2(g)?C2H2(g)△H=-Q2 kJ/mol
(3)2C(s)+2H2(g)?C2H4(g)△H=-Q3 kJ/mol
利用盖斯定律,(3)-(2),得到C2H2(g)+H2(g)?C2H4(g)△H=Q2-Q3,与题干中的a中的方程式一样,而a中的反应为放热反应,则Q2-Q3<0,所以Q2<Q3;
同理:(3)-(1)×2,得到2CH4(g)?C2H4(g)+2H2(g)△H=2Q1-Q3,与题干中的b中的方程式一样,而b中的反应为吸热反应,则2Q1-Q3>0,所以2Q1>Q3;
综上所述2Q1>Q3>Q2
故选:A.
点评 本题主要考查了盖斯定律的运用,难度不大,根据所学知识即可完成.


 科学实验活动册系列答案
科学实验活动册系列答案科目:高中化学 来源: 题型:解答题

 通过以下路线可合成(Ⅱ):
通过以下路线可合成(Ⅱ): $→_{△}^{浓H_{2}SO_{4}}$C3H4O2(Ⅲ)$\stackrel{C_{2}H_{5}OH/H+}{→}$C5H8O2$→_{一定条件}^{HBr}$(Ⅱ)
$→_{△}^{浓H_{2}SO_{4}}$C3H4O2(Ⅲ)$\stackrel{C_{2}H_{5}OH/H+}{→}$C5H8O2$→_{一定条件}^{HBr}$(Ⅱ) .
. ,反应类型是酯化反应(或取代反应).
,反应类型是酯化反应(或取代反应). .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 单位时间内生成a mo1 O2的同时生成2a mol NO2 | |
| B. | 单位时间内生成a mol O2的同时生成2a mol NO | |
| C. | 混合气体的颜色不再改变 | |
| D. | 混合气体的压强不再改变 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1mol/L Na2CO3溶液中含有0.2molNa+ | |
| B. | 在常温常压下,11.2L氮气所含的原子数目为NA | |
| C. | 2g氢气所含原子数目为NA | |
| D. | 在常温常压下,18 g水中含有的分子数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
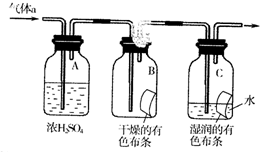 氯气是一种化学性质活泼的非金属单质,工业上
氯气是一种化学性质活泼的非金属单质,工业上查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 稀硫酸滴到铁片上:Fe+H+═Fe2++H2↑ | |
| B. | 硫酸铜溶液与氢氧化钠溶液混合:CuSO4+2OH-═Cu(OH)2↓ | |
| C. | 碳酸钠溶液与稀盐酸反应:CO32-+2H+═H2CO3 | |
| D. | 碳酸氢钠溶液与盐酸混合:HCO3-+H+═H2O+CO2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 实验室中有一未知浓度的稀盐酸,某学生为测定盐酸的浓度在实验室中进行如下实验.请你完成下列填空:
实验室中有一未知浓度的稀盐酸,某学生为测定盐酸的浓度在实验室中进行如下实验.请你完成下列填空:| 实验编号 | NaOH溶液的浓度 (mol/L) | 滴定完成时,消耗NaOH溶液的体积(mL) | 待测盐酸溶液的体积(mL) |
| 1 | 0.10 | 22.02 | 20.00 |
| 2 | 0.10 | 22.00 | 20.00 |
| 3 | 0.10 | 21.98 | 20.00 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com