
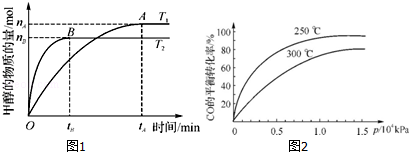
分析 (1)①根据反应速率v=$\frac{△c}{△t}$计算从反应开始到平衡生成甲醇的平均反应速率;
②温度能加快化学反应速率,能使化学平衡向着吸热方向进行;
③可逆反应达到平衡状态时,正逆反应速率相等,各组分的浓度、百分含量不再变化,据此进行判断;
④根据燃烧热的概念以及盖斯定律来计算化学反应的焓变;
(2)①根据图2可知该反应为放热反应,平衡常数与压强大小无关,只与温度有关,根据温度对化学平衡的影响判断平衡常数大小;
②根据压强对化学反应速率以及化学平衡移动的影响知识结合实际生产过程来回答.
解答 解:(1)①温度为T2时,从反应开始到平衡,生成甲醇的平均反应速率为:v(B)=$\frac{\frac{n(B)}{2L}}{{t}_{B}}$=$\frac{{n}_{B}}{2{t}_{B}}$mol/(L•min),
故答案为:$\frac{{n}_{B}}{2{t}_{B}}$mol/(L•min);
②温度能加快化学反应速率,能使化学平衡向着吸热方向进行,T2>T1,根据图一,温度升高,甲醇的物质的量减小,所以平衡逆向移动,即所以当其他条件一定时,对于该化学反应:CO2(g)+3H2(g)=CH3OH(l)+H2O(l),升高温度,反应速率加快;当其他条件一定时,升高温度,平衡逆向移动,
故答案为:当其他条件一定时,升高温度,反应速率加快;当其他条件一定时,升高温度,平衡逆向移动;
③A.该反应是一个反应前后气体系数和不同的反应,当体系压强保持不变,证明达到平衡,故A正确;
B.密闭容器中CO2、H2、CH3OH(g)、H2O(g)4种气体共存,只能证明是一个可逆反应,不能证明是平衡状态,故B错误;
C.CH3OH与H2物质的量之比为1:3,不能证明达平衡状态,故C错误;
D.每消耗1mol CO2的同时生成3molH2,能证明正逆反应速率相等,故D正确;
故答案为:AD;
④由H2(g)的燃烧热△H为-285.8kJ•mol-1知,1molH2(g)完全燃烧生成1molH2O(l)放出热量285.8kJ,该反应为:①H2(g)+$\frac{1}{2}$O2(g)=H2O(l)△H=-285.8kJ•mol-1
②CH3OH(l)+$\frac{1}{2}$O2(g)=CO2(g)+2 H2O(l)△H=-726.5kJ•mol-1,
由盖斯定律可知,3×①-②得:CO2(g)+3H2(g)?CH3OH(l)+H2O(l)△H=-130.9 kJ•mol-1,
故答案为:CO2(g)+3H2(g)=CH3OH(l)+H2O(l)△H=-130.9 kJ•mol-1;
(2)①根据CO在不同温度下的平衡转化率与压强的关系图2,可以知道该反应是一个放热反应,所以升高温度,平衡常数减小,压强大小和平衡常数之间无关,即250℃、0.5×104kPa下的平衡常数大于300℃、1.5×104kPa下的平衡常数,
故答案为:>;
②根据CO在不同温度下的平衡转化率与压强的关系图2可知,在1.3×104kPa下,CO的转化率已经很高,如果增加压强CO的转化率提高不大,而生产成本增加,得不偿失,
故答案为:在1.3×104kPa下,CO的转化率已经很高,如果增加压强CO的转化率提高不大,而生产成本增加,得不偿失.
点评 本题考查较为综合,涉及化学平衡移动的影响、化学平衡状态的判断以及化学平衡的计算知识,题目难度中等,明确化学平衡及其影响为解答关键,试题培养了学生的分析能力及化学计算能力.


 天天向上口算本系列答案
天天向上口算本系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③ | B. | ①③④ | C. | ①②④ | D. | ①②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
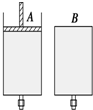 如图所示,有两只密闭容器A和B,A容器有一个移动的活塞能使容器内保持恒压,B容器能保持恒容.起始时向这两只容器中分别充入等量的体积比为2:1的SO2与O2的混合气体,并使A和B容积相等(如图).在保持400℃的条件下使之发生如下反应:2SO2(g)+O2(g)$?_{△}^{催化剂}$2SO3(g),填写下列空格.
如图所示,有两只密闭容器A和B,A容器有一个移动的活塞能使容器内保持恒压,B容器能保持恒容.起始时向这两只容器中分别充入等量的体积比为2:1的SO2与O2的混合气体,并使A和B容积相等(如图).在保持400℃的条件下使之发生如下反应:2SO2(g)+O2(g)$?_{△}^{催化剂}$2SO3(g),填写下列空格.查看答案和解析>>
科目:高中化学 来源: 题型:实验题


查看答案和解析>>
科目:高中化学 来源: 题型:选择题
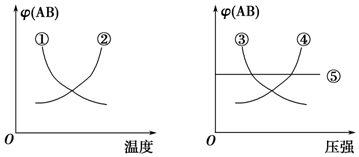
| A. | ①② | B. | ③④ | C. | ①④ | D. | ①⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1:1 | B. | 2:3 | C. | 3:2 | D. | 1:6 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com