
【题目】一定温度时,向2.0 L恒容密闭容器中充入2 mol SO2和1 mol O2,发生反应:
2SO2(g)+O2(g) ![]() 2SO3(g)。经过一段时间后达到平衡。反应过程中测定部分数据见下表:
2SO3(g)。经过一段时间后达到平衡。反应过程中测定部分数据见下表:
t / s | 0 | 2 | 4 | 6 | 8 |
n(SO3) / mol | 0 | 0. 8 | 1. 4 | 1.8 | 1.8 |
下列说法正确的是
A. 反应在前2 s 的平均速率v(O2) = 0. 4 mol·L-1·s-1
B. 保持其他条件不变,体积压缩到1.0 L,平衡常数将增大
C. 保持温度不变,向该容器中再充入2 mol SO2、1 mol O2,反应达到新平衡时n(SO3)/n(O2)增大
D. 相同温度下,起始时向容器中充入4 mol SO3,达到平衡时,SO3的转化率大于10%
【答案】C
【解析】A.根据表格中数据知,当n(SO3)=1.8mol,该反应达到平衡状态,反应在前2s的平均速率v(SO3)= 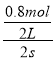 =0.2molL-1s-1,同一可逆反应中同一段时间内各物质的反应速率之比等于其计量数之比,v(O2)=
=0.2molL-1s-1,同一可逆反应中同一段时间内各物质的反应速率之比等于其计量数之比,v(O2)= ![]() ×0.2molL-1s-1=0.1molL-1s-1,故A错误;B.化学平衡常数只与温度有关,温度不变,化学平衡常数不变,与压强、物质浓度都无关,故B错误;C.温度不变,向该容器中再充入2molSO2、1molO2,增大了压强,平衡正向移动,三氧化硫的物质的量增加,氧气的物质的量减小,所以比值增大,故C正确;D.相同温度下,起始时向容器中充入4molSO3,如果三氧化硫完全转化为二氧化硫和氧气,二氧化硫和氧气的物质的量分别是4mol、2mol,为原来的2倍,增大压强平衡正向移动,则二氧化硫转化率增大,所以二氧化硫转化率大于90%,相同温度下,起始时向容器中充入4molSO3,达到平衡时,SO3的转化率小于10%,故D错误;故选C。
×0.2molL-1s-1=0.1molL-1s-1,故A错误;B.化学平衡常数只与温度有关,温度不变,化学平衡常数不变,与压强、物质浓度都无关,故B错误;C.温度不变,向该容器中再充入2molSO2、1molO2,增大了压强,平衡正向移动,三氧化硫的物质的量增加,氧气的物质的量减小,所以比值增大,故C正确;D.相同温度下,起始时向容器中充入4molSO3,如果三氧化硫完全转化为二氧化硫和氧气,二氧化硫和氧气的物质的量分别是4mol、2mol,为原来的2倍,增大压强平衡正向移动,则二氧化硫转化率增大,所以二氧化硫转化率大于90%,相同温度下,起始时向容器中充入4molSO3,达到平衡时,SO3的转化率小于10%,故D错误;故选C。


科目:高中化学 来源: 题型:
【题目】氨气在工农业生产中有着重要作用,请回答下列各有关问题。
(1)用氨气制取尿素[CO(NH2)2]的反应为:2NH3(g)+CO2(g) ![]() CO(NH2)2(l)+H2O(g) △H<0.某温度下,向容积为100L的密闭容器中通入4mol NH3和2molCO2,该反应进行到40s时达到平衡,此时CO2的转化率为50%。下图中的曲线表示该反应在前25 s内NH3浓度随时间的变化而变化。
CO(NH2)2(l)+H2O(g) △H<0.某温度下,向容积为100L的密闭容器中通入4mol NH3和2molCO2,该反应进行到40s时达到平衡,此时CO2的转化率为50%。下图中的曲线表示该反应在前25 s内NH3浓度随时间的变化而变化。

①0~25s、25s~40s内NH3的化学反应速率分别为__________、__________。存在差异的原因是______________________。
②该温度下此反应的平衡常数为_______________。
③请在图中画出反应从25s延续至60s时c(NH3)随时间变化的图像。并在其他条件不变的情况下画出使用催化剂时c(NH3)随时间的变化图像_______________
(2)尿素在一定条件下能将燃煤产生的烟气中的氮氧化物NOx转化为N2,下图表示的是尿素与某种烟气(主要为N2、NO和O2)中的NO的物质的量比值分别为1:2、2:1、3:1时,NO脱除率随温度变化的曲线

①曲线a对应CO(NH2)2与NO的物质的量的比值是______。
②CO(NH2)2与NO反应的化学方程式为________________。
③曲线a中,NO的起始浓度为6×10-4mg/m3,从A点到B点经过0.8s,该时间段内NO的脱除速率为______mg/(m3s)。
(3)希腊科学家采用高质子导电性的SYC陶瓷(能传递H+)为介质,用吸附在它外表面的金属钯多晶薄膜做电极,实现了常压、570℃条件下高转化率的电解法合成氨(装置如下图)。钯电极A是电解池的____(填“阳”或“阴”)极,该电极上的电极反应式是_________________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关物质性质的说法错误的是( )
A.热稳定性:HCl>H2S
B.原子半径:N>O
C.结合质子能力:S2﹣>Cl﹣
D.酸性:H2SO3>H2SO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【化学―选修5:有机化学基础】
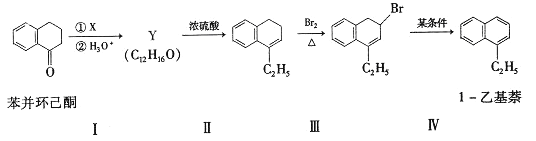
苯并环己酮是合成萘(![]() )或萘的取代物的中间体。由苯并环己酮合成1-乙基萘的一种路线如下图所示:
)或萘的取代物的中间体。由苯并环己酮合成1-乙基萘的一种路线如下图所示:
己知: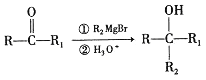
回答下列问题:
(l)萘的分子式为_______;苯并环己酮所含官能团是_______(填名称)。
(2)Y的结构简式为_________。
(3)步骤Ⅲ的反应属于_________(填反应类型)。
(4)步骤Ⅳ反应的化学方程式为____________(标明反应条件)。
(5)苯并环己酮用强氧化剂氧化可生成邻苯二甲酸。邻苯二甲酸和乙二醇经缩聚反应生成的高分子化合物的结构简式是________。
(6)1-乙基萘的同分异构体中,属于萘的取代物的有_______种(不含1-乙基萘)。W也是1 -乙基萘的同分异构体,它是含一种官能团的苯的取代物,核磁共振氢谱显示W有三种不同化学环境的氢原子,且个数比为1:1:2,W的结构简式为_________。
(7)仍以苯并环己酮为原料,上述合成路线中,只要改变其中一个步骤的反应条件和试剂,便可合成萘。完成该步骤:__________(表示方法示例:A ![]() B)。
B)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求完成下列填空:
(1)常温时,AlCl3的水溶液呈________(填“酸”、“中”、“碱”)性,原因是(用离子方程式表示):________________________。AlCl3溶液蒸干并灼烧得到的物质是__________(填化学式)。
(2)泡沫灭火器灭火时发生反应的离子方程是____________;
(3)为了使Na2S溶液中![]() 的比值变小,可加入的物质是_______
的比值变小,可加入的物质是_______
A.适量盐酸 B.适量NaOH溶液
C.适量KOH溶液 D.适量蒸馏水
(4)已知25℃ 时,Ksp[Cu(OH)2]=2×10-20,某CuSO4溶液里c(Cu2+)=0.02molL-1,如要生成Cu(OH)2 沉淀,应调整溶液的pH,使之大于______________。
(5)已知c(Ca2+)≤10-5 mol·L-1时可视为沉淀完全;Ksp(CaCO3)=4.96×10-9。在Ca(NO3)2溶液中加入(NH4)2CO3溶液后过滤,若测得滤液中c(CO![]() )=10-3 mol·L-1,则Ca2+是否沉淀完全?________(填“是”或“否”)。
)=10-3 mol·L-1,则Ca2+是否沉淀完全?________(填“是”或“否”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下的恒容容器中,可逆反应N2+3H2 ![]() 2NH3已达到平衡,下列有关说法中正确的有( )
2NH3已达到平衡,下列有关说法中正确的有( )
①1个N≡N键断裂的同时,有3个H—H键形成 ②反应混合物中各组分的体积分数保持不变 ③N2 H2的转化率一定相等 ④1个N≡N键断裂的同时,有6个N—H 键形成 ⑤气体的平均相对分子质量不再改变 ⑥N2 H2 NH3的物质的量之比一定为1∶3∶2,
A. ①②⑤ B. ①②④⑤ C. ③⑤⑥ D. ②④⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中不正确的是
A. 可用分液漏斗分离乙酸乙酯和饱和碳酸钠溶液
B. 镁着火,不能用CO2灭火
C. 毛料与棉布可以通过燃烧闻气味的方法进行鉴别
D. 容量瓶使用前必须检漏,洗涤,干燥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学习小组研究溶液中Fe2+的稳定性,进行如下实验,观察,记录结果。

实验Ⅰ
物质 | 0 min | 1min | 1h | 5h |
FeSO4 | 淡黄色 | 桔红色 | 红色 | 深红色 |
(NH4)2Fe(SO4)2 | 几乎无色 | 淡黄色 | 黄色 | 桔红色 |
(1)上述(NH4)2Fe(SO4)2溶液pH小于FeSO4的原因是________________(用化学用语表示)。溶液的稳定性:FeSO4_______(NH4)2Fe(SO4)2(填“>”或“<”) 。
(2)甲同学提出实验Ⅰ中两溶液的稳定性差异可能是(NH4)2Fe(SO4)2溶液中的NH4+保护了Fe2+,因为NH4+具有还原性。进行实验Ⅱ,否定了该观点,补全该实验。
操作 | 现象 |
取________________________, 滴加__________________,观察。 | 与实验Ⅰ中(NH4)2Fe(SO4)2溶液现象相同。 |
(3)乙同学提出实验Ⅰ中两溶液的稳定性差异是溶液酸性不同导致,进行实验Ⅲ:分别配制0.80 mol·L-1 pH为1、2、3、4的FeSO4溶液,观察,发现pH=1的FeSO4溶液长时间无明显变化,pH越大,FeSO4溶液变黄的时间越短。
资料显示:亚铁盐溶液中存在反应4Fe2++O2+10H2O ![]() 4Fe(OH)3+8H+
4Fe(OH)3+8H+
由实验III,乙同学可得出实验的结论是____________,原因是______________________。

(4)进一步研究在水溶液中Fe2+的氧化机理。测定同浓度FeSO4溶液在不同pH条件下,Fe2+的氧化速率与时间的关系如图(实验过程中溶液温度几乎无变化)。反应初期,氧化速率都逐渐增大的原因可能是______________。
(5)综合以上实验,增强Fe2+稳定性的措施有_________________。
(6)向溶液中加入一定量H2O2氧化Fe2+。为确定加入H2O2的量,需先用K2Cr2O7标准溶液滴定滤液中的Fe2+,离子方程式如下:Cr2O72-+6Fe2++14H+=2Cr3++6Fe3++7H2
①在向滴定管注入K2Cr2O7标准溶液前,滴定管需要检漏、_________ 和_______________。
②若滴定xmL滤液中的Fe2+,消耗amol·L—1K2Cr2O7标准溶液bmL,则滤液中c(Fe2+)= ___________mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C三种元素的核电荷数都小于18,它们间能形成化合物BA2、CA2,A原子最外电子层的p能级中有一个轨道填充了2个电子,B原子的最外电子层中p能级的电子数等于次外层电子总数,且A和B具有相同的电子层;C与A在周期表中位于同一主族。回答下列问题:
(1)B原子的价电子排布式_________________。
(2)CA2的分子式_________,分子构型为________________。BA2的电子式______________,分子构型为___________,其中心原子采取___________杂化。
(3)B的氢化物中分子构型为正四面体的是_____________(填名称),其中心原子的杂化方式为_____________。
(4)A的氢化物的VSEPR模型为_______,分子构型为_______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com