
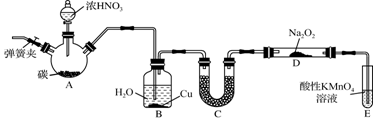
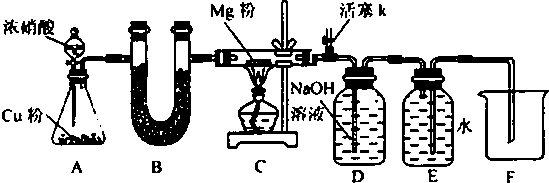
分析 Ⅰ.制备NaNO2并对其性质作探究,由实验装置可知,A中发生C+4HNO3(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+4NO2↑+2H2O,B中稀释挥发的硝酸和生成的二氧化氮,C中固体干燥剂干燥NO,并除去可能混有的酸雾,D中发生2NO+Na2O2═2NaNO2,E中高锰酸钾吸收尾气NO,据此分析解答.
解答 解:(1)A中是碳和浓硝酸发生的反应生成二氧化碳、二氧化氮和水,化学方程式为:C+4HNO3(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+4NO2↑+2H2O;
故答案为:C+4HNO3(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+4NO2↑+2H2O;
(2)B装置中的水将NO2转化为NO,铜与稀硝酸反应生成NO;
故答案为:将NO2转化为NO;铜与稀硝酸反应生成NO;
(3)A、C不能吸收酸,B、D可吸收酸且干燥气体;
故答案为:BD;
(4)由信息可知,E装置的作用是利用高锰酸钾溶液的强氧化性氧化吸收有毒气体一氧化氮,吸收有毒的NO气体,避免污染空气,反应的离子方程式为:3MnO4-+4 H++5NO=3Mn2++5NO3-+2 H2O;
故答案为:3MnO4-+4 H++5NO=3Mn2++5NO3-+2 H2O;
(5)①由信息NO能被酸性KMnO4氧化成NO3-可知,则利用NaNO2的还原性来测定其纯度,可选择的试剂是c3 mol•L-1酸性KMnO4溶液;
故答案为:E;c3 mol•L-1酸性KMnO4溶液;
②由信息酸性条件下NaNO2能把I-氧化为I2可知,则利用NaNO2的氧化性来测定其纯度的步骤是:准确称取质量为m的NaNO2样品放入锥形瓶中,加适量水溶解,加入过量的c1 mol•L-1 KI溶液、淀粉溶液,然后滴加稀硫酸,用c2 mol•L-1 Na2S2O3溶液滴定至溶液由蓝色恰好变为无色,且半分钟内不变色,读数,重复以上操作2~3次;
故答案为:c2 mol•L-1 Na2S2O3溶液;溶液由蓝色恰好变为无色.
点评 本题考查物质的制备实验,为高频考点,把握制备实验原理、实验装置的作用、氧化还原反应的应用为解答的关键,侧重分析与实验及应用能力的综合考查,题目难度中等.


科目:高中化学 来源: 题型:选择题
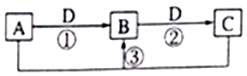 短周期元素W、X、Y、Z、Q的原子序数依次增大,已知A、B、C、D是它们两种或三种元素间形成的化合物,且A、B、C均含有Z元素.A的焰色反应呈黄色,水溶液呈弱碱性;B是两性氢氧化物;D是由W与Q形成的化合物,0.1mol•L-1D溶液的pH为1.在一定条件下它们之间的相互转化关系如图所示.下列说法正确的是( )
短周期元素W、X、Y、Z、Q的原子序数依次增大,已知A、B、C、D是它们两种或三种元素间形成的化合物,且A、B、C均含有Z元素.A的焰色反应呈黄色,水溶液呈弱碱性;B是两性氢氧化物;D是由W与Q形成的化合物,0.1mol•L-1D溶液的pH为1.在一定条件下它们之间的相互转化关系如图所示.下列说法正确的是( )| A. | X、Y、Z元素的离子半径大小是X>Y>Z | |
| B. | x元素的氢化物沸点比同主族元素的氢化物低 | |
| C. | Y与Q和W与Q元素形成的化合物化学键类型相同 | |
| D. | q的最高价氧化物对应的水化物和氢化物的酸性在同主族元素中是最强的 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
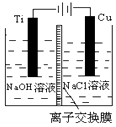 纳米级Cu2O由于具有优良的催化性能而备受关注,下表为制取纳米级Cu2O的三种方法:
纳米级Cu2O由于具有优良的催化性能而备受关注,下表为制取纳米级Cu2O的三种方法: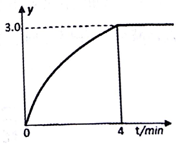
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
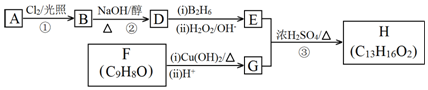
 $→_{(ii)H_{2}O_{2}/OH-}^{(i)B_{2}H_{6}}$
$→_{(ii)H_{2}O_{2}/OH-}^{(i)B_{2}H_{6}}$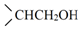
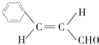 .
.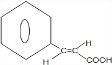 +(CH3)2CHCH2OH$?_{△}^{浓硫酸}$H2O+
+(CH3)2CHCH2OH$?_{△}^{浓硫酸}$H2O+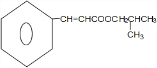 .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 6.2g白磷中所含P-P键的数目为0.15NA | |
| B. | 含H2O2 3.4克的溶液完全分解,其电子转移数目为NA | |
| C. | 117g氯化钠固体含有2NA个氯化钠分子 | |
| D. | 6克金刚石含NA个C-C键 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 人们把能够发生有效碰撞的分子叫做活化分子,同时把活化分子具有的能量叫活化能 | |
| B. | 化学反应不一定都有能量变化 | |
| C. | 活化能接近于零的反应,当反应物相互接触时,反应瞬间完成,而且温度对其反应速率几乎没有什么影响 | |
| D. | 活化能的大小不仅意味着一般分子成为活化分子的难易,也会对化学反应前后的能量变化产生影响 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙醇和丁烷都存在同分异构体 | |
| B. | (CH3CH2)2CHCH3的系统命名是2-乙基丁烷 | |
| C. | 氧气和臭氧互为同素异形体 | |
| D. | 甲烷与异戊烷互为同系物 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com