
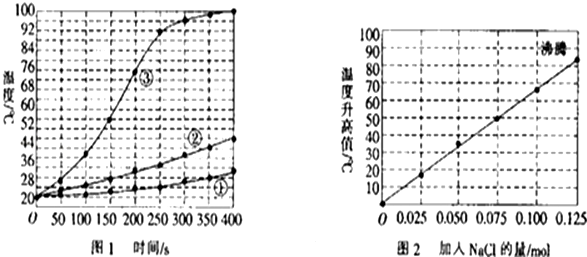
分析 (1)根据实验1中三组物质不同之处判断实验目的;
(2)结合图2可知,NaCl用量达到0.125 mol时,溶液达到沸腾状态,再增加NaCl的用量时,温度不再发生变化;
(3)根据图2当加入0.06 mol NaCl时记录的温度进行判断;
(4)根据镁粉、铁粉与NaCl水溶液共同构成了原电池的角度进行分析.
解答 解:(1)实验1中三组物质不同之处在于镁的状态,故实验1是研究的是镁的表面积与速率的关系,
故答案为:镁的表面积;
(2)根据图2可知,NaCl用量达到0.125 mol时,溶液已经达到沸腾状态,当NaCl的用量再增加时,温度不再发生变化,所以无需再做,所以B正确,
故答案为:B;
(3)由图2可见,当加入0.06 mol NaCl时,第15 min记录的温度升高值在42℃左右,所以则第15min时混合物的温度最接近于:42℃+20℃=62℃,则A正确,
故答案为:A;
(4)镁粉、铁粉与NaCl水溶液共同构成了原电池,大大促进了Mg的反应,加快了反应的速率,
故答案为:镁粉、铁粉与NaCl的水溶液构成了原电池,加快了反应速率.
点评 本题考查了探究影响化学反应速率的因素,题目难度中等,注意掌握温度、固体表面积、浓度等影响化学反应速率的因素,(4)中注意构成原电池后对反应速率的影响,试题培养了学生的分析、归纳能力及化学实验能力.


 孟建平错题本系列答案
孟建平错题本系列答案 超能学典应用题题卡系列答案
超能学典应用题题卡系列答案科目:高中化学 来源: 题型:选择题
| A. | 肯定有Na+、Al3+、Mg2+、SO42- | B. | 肯定有Na+、Mg2+、Al3+、Cl- | ||
| C. | 肯定没有Mg2+、HCO3-、MnO4-、Cl- | D. | 肯定没有K+、NH4+、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
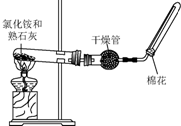 A、B、C、D是中学化学常见的四种物质,它们之间的相互转化关系如下(部分反应条件及产物略去).
A、B、C、D是中学化学常见的四种物质,它们之间的相互转化关系如下(部分反应条件及产物略去).查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 丁烷的球棍模型 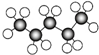 | B. | 乙烯的比例模型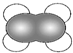 | ||
| C. | 乙醛的结构简式CH3COH | D. | 键线式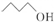 表示的有机物名称为1-戊醇 表示的有机物名称为1-戊醇 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 钠和镁分别与冷水反应,判断钠和镁金属性强弱 | |
| B. | 在MgCl2与AlCl3溶液中分别加入过量的NaOH溶液,判断镁与铝的金属性强弱 | |
| C. | 往硅酸钠溶液中通入CO2产生白色沉淀,判断碳酸与硅酸的酸性强弱 | |
| D. | 根据HF和HCl的水溶液的酸性强弱判断氟与氯的非金属性的强弱 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com