
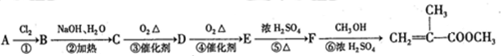
 ,
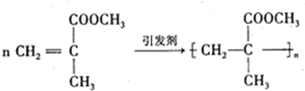
,
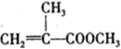 是有机玻璃的单体.下列物质属甲基丙烯酸甲酯同分异构体的是
是有机玻璃的单体.下列物质属甲基丙烯酸甲酯同分异构体的是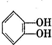 、④
、④
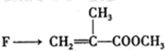
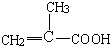 ,C连续发生氧化反应得到E,E发生消去反应生成F,故E
,C连续发生氧化反应得到E,E发生消去反应生成F,故E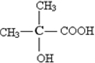 ,D为
,D为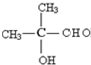 ,C为
,C为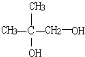 ,B为
,B为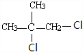 ,A为CH2=C(CH3)2,据此解答.
,A为CH2=C(CH3)2,据此解答.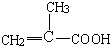 ,C连续发生氧化反应得到E,E发生消去反应生成F,故E
,C连续发生氧化反应得到E,E发生消去反应生成F,故E ,D为
,D为 ,C为
,C为 ,B为
,B为 ,A为CH2=C(CH3)2,
,A为CH2=C(CH3)2, ,故答案为:加聚反应;①④;
,故答案为:加聚反应;①④; ,故答案为:CH2=C(CH3)2;
,故答案为:CH2=C(CH3)2; ;
; ,所含官能团名称是:羧基、羟基,故答案为:羧基、羟基;
,所含官能团名称是:羧基、羟基,故答案为:羧基、羟基; )可发生银镜反应,反应方程式为:
)可发生银镜反应,反应方程式为: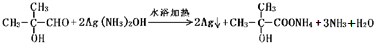 ,F发生与甲醇发生酯化反应得到甲基丙烯酸甲酯,反应方程式为:
,F发生与甲醇发生酯化反应得到甲基丙烯酸甲酯,反应方程式为: ,
,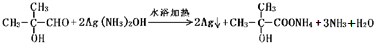 ;
; .
.


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
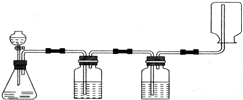 某学生在实验室做气体发生、洗涤、干燥、收集(不考虑尾气的处理)实验,装置图如图示.该同学所做的实验是( )
某学生在实验室做气体发生、洗涤、干燥、收集(不考虑尾气的处理)实验,装置图如图示.该同学所做的实验是( )| A、锌和盐酸反应制取氢气 |
| B、二氧化锰和浓盐酸反应制取氯气 |
| C、碳酸钙和盐酸反应制取二氧化碳 |
| D、过氧化钠和水反应制取氧气 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、△H1=△H2=△H3=△H4 |
| B、△H1-△H2-△H3=△H4 |
| C、△H1-△H3=△H2-△H4 |
| D、△H1>△H2>△H3>△H4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com